
【题目】回答下列各小题中的问题,请用“>”“<”或“=”填空。
(1)质量相同的下列各组物质,所含“物质的量”关系是:
①CO________CO2;
②H2SO4________H3PO4。
(2)相同物质的量的下列各组物质,比较其质量的大小:
①HCl________HF;
②HNO3________H3PO4;
③Mg________Al;
④Na+________Al3+。
(3)比较分子数目多少:
①9 g H2O________11 g CO2;
②1 g H2________1 g O2。
(4)比较下列物质中氢原子数目多少:
①4.9 g H2SO4________5.4 g H2O;
②1.6 g CH4________0.4 g H2。
【答案】(1)①> ②=
(2)①> ②< ③< ④<
3)①> ②> (4)①< ②=
【解析】根据物质的量=![]() ,(1)质量相同,物质的量与摩尔质量成反比,M(CO2)> M(CO),则n(CO)>n(CO2);M(H2SO4)=M(H3PO4),则n(H2SO4)=n(H3PO4)(2)物质的量相同,质量与摩尔质量成正比,则有m(HCl)>m(HF)、m(HNO3)<m(H3PO4)、m(Mg)<m(Al)、m(Na+)<
,(1)质量相同,物质的量与摩尔质量成反比,M(CO2)> M(CO),则n(CO)>n(CO2);M(H2SO4)=M(H3PO4),则n(H2SO4)=n(H3PO4)(2)物质的量相同,质量与摩尔质量成正比,则有m(HCl)>m(HF)、m(HNO3)<m(H3PO4)、m(Mg)<m(Al)、m(Na+)<
m(Al3+)。
(3))分子数与物质的量成正比n(H2O)=![]() =0.5 mol,n(CO2)=
=0.5 mol,n(CO2)=![]() =
=
0.2 5mol,则N(H2O)>N(CO2);n(H2)=![]() =0.5 mol,n(O2)=
=0.5 mol,n(O2)=![]() =0.03125mol,则
=0.03125mol,则
N(H2)>N(O2).
(4)n(H2SO4)=![]() =0.05 mol,n(H2O)=
=0.05 mol,n(H2O)=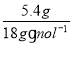 =0.3 mol,4.9 g H2SO4中氢原子个数<5.4 g H2O中氢原子个数,同理1.6 g CH4中氢原子个数等于0.4 g H2氢原子个数。
=0.3 mol,4.9 g H2SO4中氢原子个数<5.4 g H2O中氢原子个数,同理1.6 g CH4中氢原子个数等于0.4 g H2氢原子个数。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】科学家们在研制一种吸气式的锂一空气电池,工作时吸收空气中的氧气在多孔金制成正极表面上反应.总反应可表示为2Li+O2![]() Li2O2,下列有关说法正确的是( )
Li2O2,下列有关说法正确的是( )
A.充电时,多孔金制成的电极外接电源负极
B.放电时,吸收空气中22.4L的O2,就有2mol e﹣从电池负极流出
C.放电时,Li+从负极向正极移动
D.该电池可使用含Li+的水溶液作电解质溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,电解未精制饱和食盐水(含有少量Mg2+),在碳棒和铁片表面均有气体生成,一段时间后铁片附近出现浑浊现象。下列叙述正确的是

A.碳捧接直流电源的负极
B.碳棒上发生还原反应
C.铁片上的电极反应式为2Cl--2e-=Cl2↑
D.铁片附近出现的浑浊物是Mg(OH)2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C、D、E、F为前4周期的6种元素,原子序数依次增大,其中A位于周期表的s的区,其原子中电子层数和未成对电子数相同;B原子价电子排布式为nsnnpn,B和E同主族,D原子的最外层电子数是其内层的3倍;F元素位于元素周期表的第4行、第11列。试回答下列问题:
(1)基态F原子的核外电子排布式为 。
(2)关于B2A2的下列说法中正确的是 (填选项序号)。
①B2A2中的所有原子都满足8电子稳定结构
②每个B2A2分子中σ键和π键数目比为1:1
③B2A2是由极性键和非极性键构形成的非极性分子
④B2A2中心原子的杂化类型为sp杂化
(3)B、C、D三种元素第一电离能由大到小的顺序排列为 (用元素符号表示)。
(4)C的单气态氢化物与C的最高价氧化物对应的水化物反应生成一种盐H,H晶体中存在的化学键类型有 (填选项序号)。
①离子键 ②共价键 ③氢键 ④配位键 ⑤金属键
(5)基态E原子的最高能层具有的原子轨道数为 ;B和E的最高价氧化物中,熔沸点较高的是 (写化学式);
(6)F单质的晶体堆积方式为面心立方最密堆积,其配位数为 ;若F的相对分子质量为M,它的晶胞棱长为acm,则F晶体的密度为 g·cm-3。(阿伏伽德罗常数为NA)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质的性质与用途有对应关系的是
A.Si有良好的半导体性能,可以用于。
B.氨气具有还原性,可用作制冷剂
C.Na2O2呈浅黄色,可用作潜水艇中的供氧剂
D.明矾水解形成Al(OH)3胶体,可用作水处理中的净水剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(I)直接排放煤燃烧产生的烟气会引起严重的环境问题,将烟气通过装有石灰石浆液的脱硫装置可以除去其中的二氧化硫,最终生成硫酸钙。硫酸钙可在下图所示的循环燃烧装置的燃料反应器中与甲烷反应,气体产物分离出水后得到几乎不含杂质的二氧化碳,从而有利于二氧化碳的回收利用,达到减少碳排放的目的。

请回答下列问题:
(1)煤燃烧产生的烟气直接排放到空气中,引发的主要环境问题有________(填字母)。
A.温室效应 B.酸雨
C.粉尘污染 D.水体富营养化
(2)在烟气脱硫的过程中,所用的石灰石浆液在进入脱硫装置前,需通一段时间的二氧化碳,以增加其脱硫效率;脱硫时控制浆液的pH,此时浆液含有的亚硫酸氢钙可以被氧气快速氧化生成硫酸钙。
①二氧化碳与石灰石浆液反应得到的产物为_______________(填化学式)。
②亚硫酸氢钙被足量氧气氧化生成硫酸钙的化学方程式为____________________。
(II)联氨(又称肼,N2H4,无色液体)是一种应用广泛的化工原料,可用作火箭燃料,回答下列问题:
(3)联氨分子的电子式为_____________,其中氮的化合价为____________。
(4)实验室可用次氯酸钠溶液与氨反应制备联氨,反应的化学方程式为________________。
(5)①2O2(g)+N2(g)=N2O4(l) ΔH1
②N2(g)+2H2(g)=N2H4(l) ΔH2
③O2(g)+2H2(g)=2H2O(g) ΔH3
④2N2H4(l) + N2O4(l)= 3N2(g)+ 4H2O(g) ΔH4
上述反应热效应之间的关系式为ΔH4=________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com