
化学科学需要借助化学专业语言来描述,下列有关化学用语正确的是( )

科目:高中化学 来源: 题型:
已知信息:[Cu(NH3)4]SO4的电离方程式为:[Cu(NH3)4]SO4=[Cu(NH3)4]2++SO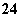 。 具有6个配体的Co3+的配合物CoClm·n NH3,若1 mol此配合物与足量的AgNO3溶液反应只生成1 mol AgCl沉淀,则m、n的值分别是( )
。 具有6个配体的Co3+的配合物CoClm·n NH3,若1 mol此配合物与足量的AgNO3溶液反应只生成1 mol AgCl沉淀,则m、n的值分别是( )
A. m=1,n=5 B. m=3,n=4 C. m=5,n=1 D. m=3,n=3
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D、E为原子序数依次增大的短周期元素。已知A、B、E三种原子最外层共有11个电子,且这三种元素的最高价氧化物对应的水化物之间两两皆能反应生成盐和水;C元素的最外层电子数比次外层电子数少4,D元素的最高正价与最低负价的代数和为4。
请回答下列问题:
(1)元素C在元素周期表中的位置是 ,元素D是 (填元素符号)。元素E是 (填名称),五种元素中离子半径最小的是 (写离子符号)。
(2)C, D, E三种元素最高价氧化物对应水化物的酸性由强到弱的顺序
为 (填化学式)。
(3)写出A和E两元素与最高价氧化物对应水化物反应的离子方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下面五种物质的沸点由高到低的顺序正确的是
①正戊烷 ②正庚烷 ③2—甲基己烷 ④3,3—二甲基戊烷 ⑤异丁烷
A.②③④①⑤ B.②①③④⑤
C.③②④①⑤ D.①②③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D、E为原子序数依次增大的短周期元素,已知A、B、E 3种原子最外层共有11个电子,且这3种元素的最高价氧化物的水化物两两皆能发生反应生成盐和水,C元素的最外层电子数比次外层电子数少4,D元素原子次外层电子数比最外层电子数多3。
(1)写出下列元素符号:B ,C ,D
(2)A与E两元素可形成化合物,用电子式表示其化合物的形成过程:
。
(3)写出A、B两元素的最高价氧化物的水化物相互反应的离子方程式:
。
(4)C、D、E的氢化物稳定性由强到弱依次为:(用化学式表示) 。
(5)D、E两元素形成化合物属 (“离子”或“共价”)化合物。其中D显最高价的化合物与水反应能生成两种酸,写出其反应方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA为阿伏加德罗常数的值,下列有关叙述正确的是
( )
A.20 mL 10 mol/L的浓硫酸与足量铜反应转移电子数为0.2NA
B.1 mol/L FeCl3溶液中Fe3+的数目小于NA
C.在精炼铜或电镀铜过程中,当阴极析出32 g铜时,转移电子数为NA
D.标准状况下,0.1NA个SO3的体积约为2.24 L
查看答案和解析>>
科目:高中化学 来源: 题型:
某硫原子的质量是a g,12C原子的质量是b g,若NA只表示阿伏加德罗常数的数值,则下列说法中正确的是( )
①该硫原子的相对原子质量为
②m g该硫原子的物质的量为 mol
mol
③该硫原子的摩尔质量是aNA g
④a g该硫原子所含的电子数为16NA
A.①③ B.②④
C.①② D.②③
查看答案和解析>>
科目:高中化学 来源: 题型:
加强空气质量检测,客观分析空气中污染物的来源及性质,将有助于制定有针对性的治理措施。下表是某城市某日的空气质量报告:
| 污染指数 | 首要污染物 | 空气质量级别 | 空气质量状况 |
| 55 | SO2 | II | 良 |
该市某校研究性学习小组对表中首要污染物SO2导致酸雨的成因进行了如下探究:
(1)用下图所示装置进行实验。
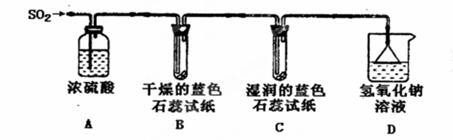
①A装置的作用是____________________。
②实验过程中,B装置内石蕊试纸的颜色没有发生变化,C装置内湿润的蓝色石蕊
试纸变成________________色,说明SO2与水反应生成一种酸,其化学反应方程式是 。
③D装置的作用是__________________________________________________,
D中发生反应的化学方程式是_________________________________________。
(2)往盛有水的烧杯中通入SO2气体,测得所得溶液的pH________7(填“>”“=”或“<”),然后每隔1h测定其pH,发现pH逐渐_______(填“变大”或“变小”), 直至恒定,原因是 (写出反应的离子方程式)。
(3)SO2形成酸雨的另一途径为:SO2与空气中的O2在飘尘的作用下反应生成SO3,SO3溶于降水生成H2SO4, 则在此过程中的飘尘是作为___________(填“催化剂”或“氧化剂”)。
(4)SO2与空气中的氧气、水反应生成硫酸而形成酸雨。该市可能易出现酸雨。
(5)汽车排放的尾气,硝酸、化肥等工业生产排出的废气中都含有氮的氧化物,氮的氧化物溶于水最终转化为__________________,是造成酸雨的另一主要原因。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com