
加强空气质量检测,客观分析空气中污染物的来源及性质,将有助于制定有针对性的治理措施。下表是某城市某日的空气质量报告:
| 污染指数 | 首要污染物 | 空气质量级别 | 空气质量状况 |
| 55 | SO2 | II | 良 |
该市某校研究性学习小组对表中首要污染物SO2导致酸雨的成因进行了如下探究:
(1)用下图所示装置进行实验。
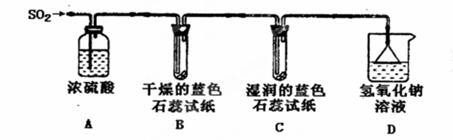
①A装置的作用是____________________。
②实验过程中,B装置内石蕊试纸的颜色没有发生变化,C装置内湿润的蓝色石蕊
试纸变成________________色,说明SO2与水反应生成一种酸,其化学反应方程式是 。
③D装置的作用是__________________________________________________,
D中发生反应的化学方程式是_________________________________________。
(2)往盛有水的烧杯中通入SO2气体,测得所得溶液的pH________7(填“>”“=”或“<”),然后每隔1h测定其pH,发现pH逐渐_______(填“变大”或“变小”), 直至恒定,原因是 (写出反应的离子方程式)。
(3)SO2形成酸雨的另一途径为:SO2与空气中的O2在飘尘的作用下反应生成SO3,SO3溶于降水生成H2SO4, 则在此过程中的飘尘是作为___________(填“催化剂”或“氧化剂”)。
(4)SO2与空气中的氧气、水反应生成硫酸而形成酸雨。该市可能易出现酸雨。
(5)汽车排放的尾气,硝酸、化肥等工业生产排出的废气中都含有氮的氧化物,氮的氧化物溶于水最终转化为__________________,是造成酸雨的另一主要原因。
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
某反应的反应物与生成物有:K2Cr2O7、KCl、CrCl3、Cl2、HCl、H2O,已知氧化性:K2Cr2O7>Cl2,则下列说法不正确的是
( )
A.Cl2是该反应的氧化产物
B.氧化剂和被氧化的还原剂的物质的量之比为1∶14
C.当转移0.2 mol电子时,被氧化的还原剂的物质的量为0.2 mol
D.由该反应可知还原性:HCl>CrCl3
查看答案和解析>>
科目:高中化学 来源: 题型:
化学与生活密切相关,下列情况会对人体健康造成较大危害的是
A.用Cl2对自来水进行消毒杀菌
B.用食醋清洗热水瓶胆内壁附着的水垢(CaCO3)
C.用SO2漂白食品
D.用小苏打(NaHCO3)发酵面团制作馒头
查看答案和解析>>
科目:高中化学 来源: 题型:
已知34Se、35Br位于同一周期,下列关系正确的是
A.热稳定性:HCl>H2Se>HBr B.还原性:Se2->S2->Cl-
C.原子半径:Se>Cl>P D.酸性:H2SeO4>H2SO4>H3PO4
查看答案和解析>>
科目:高中化学 来源: 题型:
肼(H2NNH2)是一种高能燃料,有关化学反应的能量变化如图所示。已知断裂1 mol化学键所需的能量(kJ):NN为942、OO为500、NN为154,则断裂1 mol NH键所需的能量(kJ)是( )

A.194 B.391
C.516 D.658
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:常温下,0.01 mol/L MOH溶液的pH为10,MOH(aq)与H2SO4(aq)反应生成1 mol正盐的ΔH=-24.2 kJ·mol-1,强酸与强碱的稀溶液的中和热为ΔH=-57.3 kJ·mol-1。则MOH在水溶液中电离的ΔH为( )
A.-69.4 kJ·mol-1 B.-45.2 kJ·mol-1
C.+69.4 kJ·mol-1 D.+45.2 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于粒子结构的描述不正确的是( )
A.H2S和NH3价电子总数均是8
B.次氯酸分子的结构式为:H—Cl—O
C.HS-和HCl均是含一个极性键的18电子粒子
D.1 mol D216O中含中子、质子、电子各10 NA(NA代表阿伏加德罗常数的值)
查看答案和解析>>
科目:高中化学 来源: 题型:
已知一定温度下,N2 和H2 反应生成2mol NH3时放出的热量为92.0 kJ,将此温度下的1 mol N2 和3 mol H2 放在一密闭容器中,在催化剂存在时进行反应,测得反应放出的热量为( )[忽略能量损失]
A. 一定大于92.0 kJ B. 一定等于92.0 kJ C. 一定小于92.0 kJ D. 不能确定
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com