
����Ŀ��øָ������������ܵĸ߷������ʣ���ø�Ĵ���Ӧ��ϵ�У���Ӧ����ӱ���Ϊ�������ͨ��ø�Ĵ�ת��Ϊ�������ӣ��������е�ϸ������̶���Ҫø�IJ��룬�����Ч�ʣ���ش��������⣺
��1��ø����ø����������ϸ������ʵ�ַ����ţ�����Ϊϸ���ھ��� ϵͳ����ɸ�ϵͳ�Ľṹ���еĹ��������� ����Ҷϸ����Ҳ�����ڶ�����ķ��������������ø���̲���ȡ�����б����Ƚ����ȹ����³��ƣ���һ���̵�Ŀ���� ��
��2��������Rubiconø��CO2Ũ�Ƚϸ�ʱ����ø��C2��CO2��Ӧ��Rubiconø�Ĵ��ڳ���Ϊ ����ø���С������ԡ�����O2Ũ�Ƚϸ�ʱ����ø��C2��O2��Ӧ�����ᆳһϵ�б仯���������л����CO2���䡰�����ԡ���ø�� �����ԣ���ì�ܣ�
��3����ͼ�����߱�ʾ��ø�ڲ�ͬ�¶��±����㹻��ʱ�䣬����ø������ߵ��¶��²������ø���ԣ���ͼ�ɵó��� ��Ϊ����֤��һ���ۣ��������µ���ά�طֽ�øΪʵ����ϣ��Ƚ��ڵ��º������¶��´����ø���Ե�Ӱ�죬д��ʵ�����˼·�� ��

���𰸡���1������Ĥ ѡ������ ����ʹ������øʧ��
��2��Ҷ������� רһ��
��3��ø�ڽϵ��¶��´��������Ӱ��С���ڽϸ��¶��´��������Ӱ���
�����µ���ά�طֽ�ø�ֱ��ڵ��º������¶��´����㹻��ʱ������������¶��²��������
��������
�����������1��ø����ø����������ϸ������ʵ�ַ����ţ�����Ϊϸ���ھ�������Ĥϵͳ������Ĥ�Ľṹ�Ĺ���������ѡ�����ԣ��̲���ȡ�����б����Ƚ����ȹ����³��ƣ���һ���̵�Ŀ���Ǹ���ʹ������øʧ�
��2��������Rubiconø��CO2Ũ�Ƚϸ�ʱ����ø��C2��CO2��Ӧ���÷�Ӧ���ڰ���Ӧ�е����ʱ仯�����Rubiconø�Ĵ��ڳ���ΪҶ������ʣ���ø���С������ԡ�����O2Ũ�Ƚϸ�ʱ����ø��C2��O2��Ӧ�����ᆳһϵ�б仯���������л����CO2���䡰�����ԡ���ø��רһ����ì�ܣ�
��3����ͼ�����߱�ʾ��ø�ڲ�ͬ�¶��±����㹻��ʱ�䣬����ø������ߵ��¶��²������ø���ԣ���ͼ�ɵó�ø�ڽϵ��¶��´��������Ӱ��С���ڽϸ��¶��´��������Ӱ���Ϊ����֤��һ���ۣ����Խ����µ���ά�طֽ�ø�ֱ��ڵ��º������¶��´����㹻��ʱ������������¶��²�������ԣ�
�ʴ�Ϊ����1������Ĥ ѡ������ ����ʹ������øʧ��
��2��Ҷ������� רһ��
��3��ø�ڽϵ��¶��´��������Ӱ��С���ڽϸ��¶��´��������Ӱ���
�����µ���ά�طֽ�ø�ֱ��ڵ��º������¶��´����㹻��ʱ������������¶��²��������


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���о���ԱΪ�˱Ƚϼס��ҡ������������������ĵ���ø����ȡҺ��ø����Ũ����ͬ���Ļ��ԣ�����������ʵ�飺
�����Լ���mL�� | �Թ�1 | �Թ�2 | �Թ�3 | �Թ�4 |
����ˮ | 2 | 2 | 2 | A |
pH=8����Һ | 0.5 | 0.5 | 0.5 | 0.5 |
������Һ | 1 | 1 | 1 | 1 |
��������ȡҺ | 0.3 | |||
��������ȡҺ | 0.3 | |||
��������ȡҺ | 0.3 | |||
����� | 3.8 | 3.8 | 3.8 | B |
������±���ע����+����ɫ����++����ɫ�������������ɫ����������ش��������⣺
�Թ�1 | �Թ�2 | �Թ�3 | �Թ�4 | |
��ɫ��dz�� | ++ | �� | + | C |
��1������A����ֵΪ ��C����ɫ��dz�̶� ���á�+��������ʾ����
��2����ʵ����Ա����� ���ر����� ��д��2�ּ��ɣ���
��3�������õ�Һ������۵�ʣ�������ж�ʵ�����⣬�������� �Լ��������������������ø��Լ����飬��ɫ�仯������Թ��� ��
��4��������������ó��Ľ����ǣ���ͬ��Դ�ĵ���ø����Ȼø����Ũ����ͬ�������Բ�ͬ�����ʵ��������ø���Բ���ĸ���ԭ���� ��
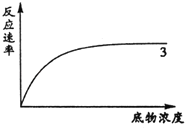
��5��ͬѧ�ǻ����˷�Ӧ���������Ũ�ȹ�ϵ��ʵ�飮�����������Ѹ���ʵ��������3���Թ���ø���Ե����ߣ������������л���2���Թ���ø���Ե����ߣ� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ʲ����ɵ���ֱ�ӻ������ɵ���
A. NO2 B. Na2O2 C. SO2 D. FeCl3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ȷ���ǣ� ��
A.������NO2����ɫ���壬����ˮ������Ӧ
B.SiO2������ˮ��������NaOH��Һ��Ӧ
C.Ũ��������ͭ��Ӧ����H2
D.ʵ���ҳ���NH4Cl��Ca��OH��2���������������ȡNH3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й���Na2O��Na2O2��˵���У�����ȷ����
A. ������2�۵���Ԫ�� B. ��ɫ��Ӧ��Ϊ��ɫ
C. ��ˮ��Ӧ������NaOH D. �������̼��Ӧ������Na2CO3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����в����ϰ�ȫ�淶���ǣ� ��
A.�������Ż�ʱʹ����ĭ��������
B.NH3й¶ʱ���������ˮ��
C.��Cl2��β���ü���Һ���������ŷ�
D.�����������Ӧ�Ͻ��̻�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B��C��D��E���������о�����ͬһ�ַǽ���Ԫ�أ������ܷ�����ͼ��ʾ��ת����ϵ������Ԫ����R��ʾ����AΪR�������D��NaOH��Һ��Ӧ����C��H2 �� 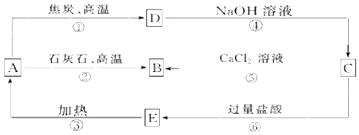
��ش�
��1��д����Ӧ���ʵĻ�ѧʽ��A�� C�� E
��2����Ӧ�ٵĻ�ѧ����ʽΪ�� ��
��3����Ӧ�ܵ����ӷ���ʽΪ�� ��
��4��H2CO3������ǿ��E�ģ��������ӷ���ʽ����֤���� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������ƣ�Na2S2O5���dz��õ�ʳƷ��������֮һ��ij�о�С���������ʵ�飺������ͼ1װ�ã�ʵ��ǰ�ѳ���װ���ڵĿ�������ȡNa2S2O5 �� ��֪����װ�â�����Na2S2O5���������������ķ�ӦΪNa2SO3+SO2�TNa2S2O5 ��
��Na2S2O5�����ڿ����б���������Na2SO4 �� 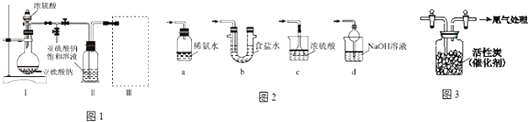
��1��װ�â��в�������Ļ�ѧ����ʽΪ ��
��2��Ҫ��װ�â��л���������ľ��壬�ɲ�ȡ�ķ��뷽���� ��
��3��װ�â����ڴ���β������ѡ�õ������װ�ã�ͼ2�����г���������ȥ��Ϊ������ţ���
��4�����Na2S2O5�����ڿ������ѱ�������ʵ�鷽���� ��
��5��Ϊ���о������Cl2�����SO2��Ӧ�����г̶ȣ�����ͼ3��ʾװ���ռ��������Cl2 �� ��ͨ�����SO2 �� ����ƿ������������ɫҺ��SO2Cl2 �� ��ַ�Ӧ��Һ���ʣ��������룮������NaOH��Һ���շ���������壬������ϡ�����ữ���ٵμ�BaCl2��Һ��������ɫ�������ð�ɫ������ �� �ɴ˿�֪��Ӧ��ʣ������Ȼ�������壬�ۺ�ʵ����Ϣ����д�������SO2��Cl2��Ӧ�Ļ�ѧ����ʽ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪:2CO(g)+O2(g)=2CO2(g) ��H=-566kJ/mol Na2O2(s)+CO2(g)=Na2CO3(s)+1/2O2(g) ��H=-226kJ/mol�����������Ȼ�ѧ����ʽ�жϣ�����˵����ȷ����
A. CO��ȼ����Ϊ-283kJ/mol
B. ��ͼ�ɱ�ʾ��CO����CO2�ķ�Ӧ���̺�������ϵ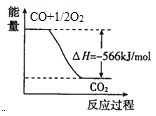
C. 2Na2O2(s)+2CO2(s)=Na2CO3(s)+O2(g) ��H>-452kJ/mol
D. CO(g)��Na2O2(s)��Ӧ�ų�509kJ����ʱ��ת�Ƶ��Ӹ���Ϊ6.02��1023
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com