
��1����һ�������£���1.00molN2(g����3.00molH2(g�������һ��10.0L�ܱ������У��ڲ�ͬ�¶��´ﵽƽ��ʱNH3(g����ƽ��Ũ����ͼ��ʾ�������¶�ΪT1ʱƽ���������а������������Ϊ25.0%��

��1�����¶���T1�仯��T2ʱ��ƽ�ⳣ����ϵK1 K2������������������������ʱ��H 0���������������
��2���÷�Ӧ��T1�¶���5.0min�ﵽƽ�⣬���ʱ����N2�Ļ�ѧ��Ӧ����Ϊ ��N2��ת����
��3��T1�¶��¸÷�Ӧ�Ļ�ѧƽ�ⳣ��K1�� ��
��4��500��ʱ,����ø�¯��c(N2��=0��5mol/L��c(H2��=0.5mol/L�� c(NH3��=0.5mol/L����������£��÷�Ӧ�Ƿ���ƽ��״̬______(���ǻ��,��ʱ��Ӧ������v��________v��(�� >, <, =��.
��5�����������о��������ڳ��³�ѹ����������N2�ڴ���������ˮ������Ӧ��
2N2(g����6H2O(l����4NH3(g����3O2(g�����˷�Ӧ�ġ�S 0���������������
��֪����2CO(g����2NO(g��=N2(g����2CO2(g�� ��H=��a kJ��mol-1
��2NO(g����O2(g��=2NO2(g�� ��H=��b kJ��mol-1��
��CO��ȼ���ȡ�H =��c kJ��mol-1��
д����������β����NO2����Ⱦʱ��NO2��CO�ķ�Ӧ���Ȼ�ѧ��Ӧ����ʽ
 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��ӱ�ʡ��һ�ϵ�һ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
�������ӷ���ʽֻ�ܱ�ʾһ����ѧ��Ӧ����
A��H+ + OH�� = H2O
B��Cl��+ Ag+ = AgCl��
C��Cu2++2OH��+Ba2++SO42��= BaSO4��+Cu(OH)2��
D��H+ + SO42�� + OH��+ Ba2+ = BaSO4��+ H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ����������������и�һ�����в��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
24 mLŨ��Ϊ0.05mol��L ��1��Na2SO3��Һǡ����20mLŨ��
��1��Na2SO3��Һǡ����20mLŨ�� Ϊ0.02mol��L��1��K2Cr2O7��Һ��ȫ��Ӧ����֪Na2SO3��K2Cr2O7����ΪNa2SO4����Ԫ��Cr�ڻ�ԭ�����еĻ��ϼ�Ϊ
Ϊ0.02mol��L��1��K2Cr2O7��Һ��ȫ��Ӧ����֪Na2SO3��K2Cr2O7����ΪNa2SO4����Ԫ��Cr�ڻ�ԭ�����еĻ��ϼ�Ϊ
A����2�� B����3�� C����4�� D����5��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�꽭��ʡ��һ�ϵڶ��ζο���ѧ�Ծ��������棩 ���ͣ�ѡ����
��ѧʵ�����ע�ⰲȫ�������������ڰ�ȫ��������
A��������ԭ����ͭʵ���У���ͨ�������������ͭ
B���������ὦ�����У�Ӧ������ˮ��ϴ����ϴ��գ�۾�
C��ʵ����������еķ�Һ������ˮ���ų�ʵ���ң�������Ⱦʵ����
D����������ʱ��ˮ���ռ���������ֵ������������ɿ��Թ��ϵ���Ƥ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�꽭��ʡ�߶��ϵ�һ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
��22.4 g������ȫ�ܽ���ijŨ�ȵ������У��練Ӧֻ�ռ���0.3 mol NO2��0.2 mol NO������˵����ȷ����
A����Ӧ�����ɵ���ֻΪFe(NO3)3
B����Ӧ�����ɵ���ֻΪFe(NO3)2
C����Ӧ�����ɵ���ΪFe(NO3)3��Fe(NO3)2�������ʵ���֮��Ϊ1��3
D����Ӧ�����ɵ���ΪFe(NO3)3��Fe(NO3)2�������ʵ���֮��Ϊ3��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ������������ѧ�߶���ѧ�����в��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
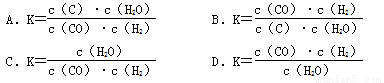
���ڿ��淴Ӧ��C(s����H2O(g�� CO(g����H2(g������һ���¶��´ﵽƽ��ʱ����ƽ�ⳣ������ʽ��ȷ��
CO(g����H2(g������һ���¶��´ﵽƽ��ʱ����ƽ�ⳣ������ʽ��ȷ�� ��
��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ������������ѧ�߶���ѧ�����в��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�����½�1mol��CuSO4��5H2O(s������ˮ��ʹ��Һ�¶Ƚ��ͣ���ЧӦΪ��H1����1mol��CuSO4(s������ˮ��ʹ��Һ�¶����ߣ���ЧӦΪ��H2��CuSO4��5H2O���ȷֽ�Ļ�ѧ����ʽΪ��CuSO4��5H2O(s��= CuSO4(s��+5H2O(l���� ��ЧӦΪ��H3���������ж���ȷ����
A����H2����H3 B����H1����H3
C����H1 =��H2+��H3 D����H1+��H2 ����H3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016��ӱ�ʡ������ѧ�����в��Ի�ѧ�Ծ��������棩 ���ͣ������
��1��������Գ���ر���Ϊ����ɫ��ѧ��Դ�����䡢�ŵ�ʱ�ķ�Ӧ��
2Ni(OH)2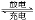 2NiO(OH) + H2�ŵ�ʱ�������ĵ缫��ӦʽΪ �����ʱ���õ缫Ӧ���Դ�� ���������������������
2NiO(OH) + H2�ŵ�ʱ�������ĵ缫��ӦʽΪ �����ʱ���õ缫Ӧ���Դ�� ���������������������
��2�����ڿ�����ȼ�գ�����ˮ�͵�������֪��N2(g)+3H2(g)  2NH3(g) ��H= ��92.4kJ��mol-1, 2H2(g)+O2(g)
2NH3(g) ��H= ��92.4kJ��mol-1, 2H2(g)+O2(g) 2H2O(l) ��H=-572 kJ��mol-1�����ڿ�����ȼ������Һ̬ˮ�͵���ʱ���Ȼ�ѧ����ʽΪ�� ��
2H2O(l) ��H=-572 kJ��mol-1�����ڿ�����ȼ������Һ̬ˮ�͵���ʱ���Ȼ�ѧ����ʽΪ�� ��
��3���о�������ҵ�Ϻϳɰ���Ӧ��N2(g)+3H2(g)  2NH3(g)�����ݻ��̶����ܱ������з���������Ӧ����һ��Ϊ�������ڲ�ͬʱ�̵�Ũ�ȡ�
2NH3(g)�����ݻ��̶����ܱ������з���������Ӧ����һ��Ϊ�������ڲ�ͬʱ�̵�Ũ�ȡ�
ʱ��/min | c(N2)/mol��L��1 | c(H2) /mol��L��1 | c(NH3) /mol��L��1 |
0 | 0.6 | 1.8 | 0 |
5 | 0.48 | X | 0.24 |
10 | 0.26 | 0.78 | 0.68 |
��һ
0��5 min��H2��ƽ����Ӧ����vH2= ����Ӧ��5����ʱ�����������˸ı䣬�ı������������ ������ţ���
a������������Ũ�� b�������¶� c��ʹ�ô��� d�������NH3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�긣��ʡ�����и߶������У��ģ���ѧ�Ծ��������棩 ���ͣ�ѡ����
2013���붬����������س��������������������������ڼ���������������
A��¶��������� B��������չ��������
C���ҿ��ķ���ľ D����������̫����
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com