
| ||
| A、5:3 | B、5:4 |
| C、1:1 | D、3:5 |


 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案 英才计划同步课时高效训练系列答案
英才计划同步课时高效训练系列答案科目:高中化学 来源: 题型:
| A、40 | B、42 | C、44 | D、46 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 分子式 | 结构简式 | 外观 | 熔点 | 溶解性 |
| C12H10ClN3O |  | 白色结晶粉末 | 170~172℃ | 易溶于水 |

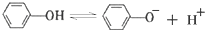 ,苯酚的酸性大于
,苯酚的酸性大于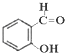 (邻羟基苯甲醛),其原因是
(邻羟基苯甲醛),其原因是查看答案和解析>>
科目:高中化学 来源: 题型:
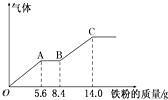 某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份.向其中一份中逐渐加入铜粉,最多能溶解9.6g.向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示(已知硝酸只被还原为NO气体).下列分析或结果错误的是( )
某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份.向其中一份中逐渐加入铜粉,最多能溶解9.6g.向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示(已知硝酸只被还原为NO气体).下列分析或结果错误的是( )| A、原混合酸中HNO3的物质的量为0.1 mol |
| B、OA段产生的是NO,AB段的反应为Fe+2Fe3+═3Fe2+,BC段产生氢气 |
| C、第二份溶液中最终溶质为FeSO4 |
| D、H2SO4浓度为2.5 mol?L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、25℃时,饱和Mg(OH)2溶液与饱和MgF2溶液相比,前者的c(Mg2+)大 |
| B、25℃时,Mg(OH)2的悬浊液加入少量的NH4Cl固体,c(Mg2+)增大 |
| C、25℃时,Mg(OH)2固体在20 mL 0.01 mol?L-1氨水中的Ksp比在20 mL 0.01 mol?L-1NH4Cl溶液中的Ksp小 |
| D、25℃时,在Mg(OH)2的悬浊液中加入NaF溶液后,Mg(OH)2不可能转化成为MgF2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、标准状况下,1.8 g H2O所含有的质子数为NA |
| B、1 L 1 mol/L的Na2CO3溶液中含有的CO32-数目为NA |
| C、25℃时,1 L pH=13的 Ba(OH)2溶液中含有的OH-数目为0.2NA |
| D、标准状况下,2.24 L 氯气与过量的氢氧化钠溶液完全反应转移的电子数为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
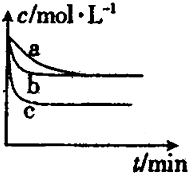 1000℃时,硫酸钠可与氢气发生反应:Na2SO4(s)+4H2(g)?Na2S(s)+4H2O(g).请回答下列问题:
1000℃时,硫酸钠可与氢气发生反应:Na2SO4(s)+4H2(g)?Na2S(s)+4H2O(g).请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在一定温度压强下,14 gN2所含的体积可能为11.2 L |
| B、标准状况下,足量NaOH溶液与2.24 LCl2反应,转移电子数目为0.1NA |
| C、标准状况下,11.2 LH2O中含有的电子数为5NA |
| D、加热条件下,足量Cl2与1 molFe粉充分反应,转移的电子数为3NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com