
【题目】一定温度下,在冰醋酸加水稀释的过程中,溶液的导电能力(I)随着加入水的体积V变化的曲线如图所示。下列说法正确的是( )
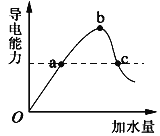
A.a、c两点pH不同
B.向c溶液中加水,溶液中所有离子浓度都减小
C.误用湿润的pH试纸测b点pH结果偏大
D.![]() b点大于c点
b点大于c点
科目:高中化学 来源: 题型:
【题目】在反应3S+6KOH=2K2S+K2SO3+3H2O中,被还原的硫和被氧化的硫的质量比为:
A. 2:1 B. 1:2 C. 3:1 D. 1:3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中不正确的是
A. 食醋中含有乙酸,乙酸可由乙醇氧化得到
B. 乙醇、乙酸乙酯、乙酸能用饱和碳酸钠溶液鉴别
C. 乙酸、乙酸乙酯、葡萄糖和淀粉的最简式相同
D. 生活中食用的食醋、植物油、动物蛋白等都是混合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关2L0.2mol·L-1K2SO4溶液的叙述,正确的是
A.含有0.2molK2SO4
B.K+的物质的量浓度为0.2mol·L-1
C.K+的物质的量为0.8mol
D.取出1LK2SO4溶液后,剩余K2SO4溶液的浓度变为0.1mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1L某混合溶液中可能含有的离子如下表:
可能大量含有的阳离子 | H+、NH4+ 、Al3+、K+ |
可能大量含有的阴离子 | Cl﹣、Br﹣、I﹣、ClO﹣、AlO2﹣ |
(1)往该溶液中逐滴加入NaOH溶液并适当加热,产生沉淀和气体的物质的量(n)与加入NaOH溶液的体积(v)的关系如图所示.
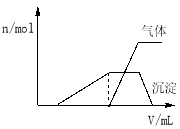
①则该溶液中确定含有的离子有 ;
②不能确定是否含有的阳离子有 ;
③要确定其存在可补充做的实验是 ;
④肯定不存在的阴离子有 .
(2)经检测,该溶液中含有大量的Cl﹣、Br﹣、I﹣,若向1L该混合溶液中通入一定量的Cl2,溶液中Cl﹣、Br﹣、I﹣的物质的量与通入Cl2的体积(标准状况)的关系如下表所示,分析后回答下列问题:
Cl2的体积(标准状况) | 2.8L | 5.6L | 11.2L |
n(Cl﹣) | 1.25mol | 1.5mol | 2mol |
n(Br﹣) | 1.5mol | 1.4mol | 0.9mol |
n(I﹣) | a mol | 0 | 0 |
①当通入Cl2的体积为2.8L时,溶液中发生反应的离子方程式为 .
②原溶液中Cl﹣、Br﹣、I﹣的物质的量浓度之比为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“绿色化学”对化学反应提出了“原子经济性”(原子节约) 的新概念及要求,理想原子经济性反应是原料分子中的原子全部转化成所需要的产物,不产生副产物,实现零排放。下列反应类型一定符合这一要求的是
①取代反应 ②加成反应 ③水解反应 ④加聚反应 ⑤酯化反应
A. ②④ B. ②③ C. ④⑤ D. ①④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿佛加德罗常数,下列对于0.3mol/L的硫酸钾溶液的说法中不正确的是( )
A. 1L溶液中含有0.6NA个钾离子
B. 1L溶液中含有钾离子和硫酸根离子总数为0.9NA
C. 2L溶液中钾离子浓度为1.2mol/L
D. 2L溶液中含有硫酸根离子0.6NA个
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向含有0.1 mol·L-1 AlCl3和0.3 mol·L-1 NH4Cl的混合液1 L中加入0.1 mol·L-1 NaOH溶液 (纵坐标为沉淀的物质的量,横坐标为加入试剂的体积)正确的是( )

A. A B. B C. C D. D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com