
���ݵ���������Ӧ���Ȼ�ѧ����ʽ
(i) I2(g)+ H2(g)  2HI(g)+ 9.48 kJ (ii) I2(S)+ H2(g)
2HI(g)+ 9.48 kJ (ii) I2(S)+ H2(g) 2HI(g) - 26.48 kJ
2HI(g) - 26.48 kJ
�����ж���ȷ����
A��254g I2(g)��ͨ��2gH2(g)����Ӧ����9.48 kJ
B��1 mol��̬����1 mol��̬���������������17.00 kJ
C����Ӧ(i)�IJ���ȷ�Ӧ(ii)�IJ����ȶ�
D����Ӧ(ii)�ķ�Ӧ���������ȷ�Ӧ(i)�ķ�Ӧ����������

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ij��Ӧ���������仯��ͼ��ʾ������˵����ȷ����(����)
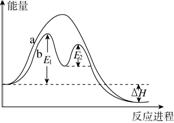
A����Ӧ����a�д�������
B���÷�ӦΪ���ȷ�Ӧ����ЧӦ���ڦ�H
C���ı�������ɸı�÷�Ӧ�Ļ��
D���д��������£���Ӧ�Ļ�ܵ���E1��E2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
NH3��һϵ�з�Ӧ���Եõ�HNO3��NH4NO3������ͼ��ʾ��
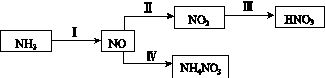
(1)���У�NH3��O2�ڴ��������·�Ӧ���仯ѧ����ʽ��_________________________��
(2)����2NO(g)��O2(g)  2NO2(g)��������������
2NO2(g)��������������
ͬʱ���ֱ���NO��ƽ��ת�����ڲ�ͬѹǿ(p1��p2)�����¶ȱ仯������(��ͼ)��
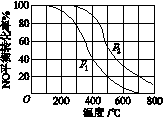
�ٱȽ�p1��p2�Ĵ�С��ϵ��________��
�����¶����ߣ��÷�Ӧƽ�ⳣ���仯��������________��
(3)���У������¶ȣ���NO2(g)ת��ΪN2O4(l)�����Ʊ�Ũ���ᡣ
����֪��2NO2(g)  N2O4(g)����H1 2NO2(g)
N2O4(g)����H1 2NO2(g) N2O4(l)����H2
N2O4(l)����H2
���������仯ʾ��ͼ�У���ȷ����(ѡ����ĸ)________��
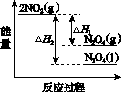 ��
��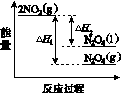
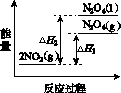
������A������������������B C
��N2O4��O2��H2O���ϵĻ�ѧ����ʽ��________________________________________��
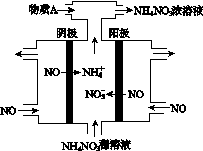
(4)���У����NO�Ʊ�NH4NO3���乤��ԭ����ͼ��ʾ��Ϊʹ������ȫ��ת��ΪNH4NO3���貹��A��A��________��˵�����ɣ�________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��ӦA+B��C(��H<0)���������У���A+B��X(��H>0)����X��C(��H<0)������ʾ��ͼ�У�����ȷ��ʾ�ܷ�Ӧ�����������仯����


A B C D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
25�桢101kPa �£���2Na(s)��1/2O2(g)=Na2O(s) ��H1=��414KJ/mol
��2Na(s)��O2(g)=Na2O2(s) ��H2=��511KJ/mol
����˵����ȷ����
A.�ٺ͢ڲ�����������Ӹ����Ȳ����
B.�ٺ͢����ɵ����ʵ����IJ��ת�Ƶ�������ͬ
C.������Na������O2��Ӧ����Na2O�����¶���������Na2O�������ӿ�
D.25�桢101kPa �£�Na2O2��s��+2 Na��s��= 2Na2O��s�� ��H=��317kJ/mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��298K��100kPaʱ����֪��2 �S
�S
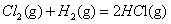 �S
�S
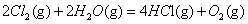 �S
�S
��S ��S
��S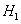 �ͨS
�ͨS ��Ĺ�ϵ��ȷ����
��Ĺ�ϵ��ȷ����
A .�S =�S
=�S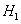 +2�S
+2�S B �S
B �S =�S
=�S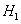 +�S
+�S
C. �S =�S
=�S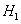 -2�S
-2�S D. �S
D. �S =�S
=�S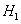 - �S
- �S
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���ᣨH3BO3����ʳƷ��ҽҩ����Ӧ�ù㷺��
(1)�����B2H6������ˮ��Ӧ�Ļ�ѧ����ʽ��B2H6 + 6H2O=2H3BO3 +________��
(2)������������ͬʱ����ӦH3BO3 +3CH3OH B(OCH3)3 +3H2O�У�H3BO 3��ת���ʣ�
B(OCH3)3 +3H2O�У�H3BO 3��ת���ʣ�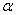 ���ڲ�ͬ�¶����淴Ӧʱ�䣨t���ı仯��ͼ12���ɴ�ͼ�ɵó���
���ڲ�ͬ�¶����淴Ӧʱ�䣨t���ı仯��ͼ12���ɴ�ͼ�ɵó���
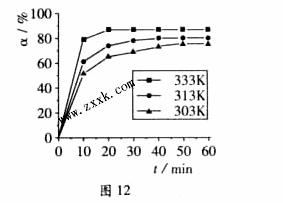
���¶ȶ�Ӧ�÷�Ӧ�ķ�Ӧ���ʺ�ƽ���ƶ���Ӱ����____ ___
�ڸ÷�Ӧ��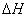 _____0(�<������=����>��).
_____0(�<������=����>��).
(3)H3BO 3��Һ�д������·�Ӧ��
H3BO 3��aq��+H2O��l�� [B(OH)4]-( aq)+H+��aq����֪0.70 mol��L-1 H3BO 3��Һ�У�������Ӧ��298K�ﵽƽ��ʱ��cƽ����H+��=2. 0 �� 10-5mol��L-1��cƽ����H3BO 3����c��ʼ��H3BO 3����ˮ�ĵ����
[B(OH)4]-( aq)+H+��aq����֪0.70 mol��L-1 H3BO 3��Һ�У�������Ӧ��298K�ﵽƽ��ʱ��cƽ����H+��=2. 0 �� 10-5mol��L-1��cƽ����H3BO 3����c��ʼ��H3BO 3����ˮ�ĵ���� ���Բ��ƣ�����¶��¸÷�Ӧ��ƽ�ⳣ��K��H2O��ƽ��Ũ��������K�ı���ʽ�У�������������λ��Ч���֣�
���Բ��ƣ�����¶��¸÷�Ӧ��ƽ�ⳣ��K��H2O��ƽ��Ũ��������K�ı���ʽ�У�������������λ��Ч���֣�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�ڼס��ҡ��������ĸ��ձ��ڷֱ����0.1mol���ơ������ơ��������ƺ��������ƣ�Ȼ�������100mLˮ�����裬ʹ������ȫ�ܽ⣬��ס��ҡ�������������Һ�����ʵ�����������С˳���� �� ��
A���ף��ң������� B�������ף���=��
C����=������=�� D�������ף��ң���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�ڱ�״���£�CO��CO2�Ļ�����干67.2L������Ϊ116g����
��1��������������ʵ���֮��Ϊ����mol��
��2������CO2���� mol��
��3��CO���������Ϊ���٣�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com