
已知A、B、C、D和E 5种分子所含原子数目依次为1、2、3、4和6,且都含有18个电子。又知B、C和D是由两种元素的原子组成。请回答:
(1)组成A分子的原子的核外电子排布式是 ;
(2)B和C的分子式分别是 和 ;C分子的立体结构呈 形,该分子属于 分子(填“极性”或“非极性”);
(3)若向D的稀溶液中加入少量二氧化锰,有无色气体生成。则D的分子式是 ,该反应的化学方程式为 ;
(4)若将1mol E在氧气中完全燃烧,只生成1mol CO2和2molH2O,则E的分子式是 。
【答案】
(1)1s22s22p63s23p6
(2)HCl H2S V 极性
(3)H2O2 2H2O2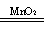 2H2O+O2↑
2H2O+O2↑
(4)CH4O (答CH3OH也可)
【解析】由题意知A是Ar,电子排布式是1s22s22p63s23p6。B、C有两种元素的原子组成,且原子数目分别为2,3,则B为HCl,C为H2S。又因D18个电子,4个原子组成,稀溶液中加入少量MnO2有气体生成,则D为H2O2,2H2O2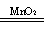 2H2O+O2↑。1 mol E在氧气中燃烧只生成1 mol CO2和2 mol H2O,说明E分子中含有1个C原子、4个氢原子,由18个电子还必须有1个O原子,故E分子式为CH4O。
2H2O+O2↑。1 mol E在氧气中燃烧只生成1 mol CO2和2 mol H2O,说明E分子中含有1个C原子、4个氢原子,由18个电子还必须有1个O原子,故E分子式为CH4O。


 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案科目:高中化学 来源: 题型:
氧是地壳中含量最多的元素。
(1)氧元素基态原子核外未成对电子数为 个。
(2)H2O分子内的O-H键、分子间的范德华力和氢键从强到弱依次为 。
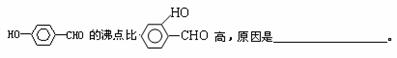
(3) H+可与H2O形成H3O+,H3O+中O原子采用 杂化。H3O+中H-O-H键角比H2O中H-O-H键角大,原因为 。
(4)CaO与NaCl的晶胞同为面心立方结构,已知CaO晶体密度为ag·cm-3,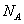 表示阿伏加德罗常数,则CaO晶胞体积为 cm3。
表示阿伏加德罗常数,则CaO晶胞体积为 cm3。
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z、Q、E五种元素中,X原子核外的M层中只有两对成对电子,Y原子核外的L层电子数是K层的两倍,Z是地壳内含量(质量分数)最高的元素,Q的核电荷数是X与Z的核电荷数之和,E在元素周期表的各元素中电负性最大。请回答下列问题:
(1)X、Y的元素符号依次为 、 ;
(2)XZ2与YZ2分子的立体结构分别是 和 ,相同条件下两者在水中的溶解度较大的是 (写分子式),理由是 ;
(3)Q的元素符号是 ,它属于第 周期,它的核外电子排布式为 ,在形成化合物时它的最高化合价为 ;
(4)用氢键表示式写出E的氢化物溶液中存在的所有氢键 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关化学键与晶体结构说法正确的是
A 两种元素组成的分子中一定只有极性键
B 离子化合物的熔点一定比共价化合物的高
C 非金属元素组成的化合物一定是共价化合物
D 含有阴离子的化合物一定含有阳离子
查看答案和解析>>
科目:高中化学 来源: 题型:
.A、B、C、D、E代表5种元素。请填空:
(1)A元素基态原子的最外层有3个未成对电子,次外层有2个电子,其元素符号为 ;
(2)B元素的负一价离子和C元素的正一价离子的电子层结构都与氩相同,B的元素符号为 ,C的元素符号为 ;
(3)D元素的正三价离子的3d亚层为半充满,D的元素符号为 ,其基态原子的电子排布式为 。
(4)E元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,E的元素符号为 ,其基态原子的电子排布式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是
A NH3是极性分子,分子中N原子是在3个H原子所组成的三角形的中心
B CCl4是非极性分子,分子中C原子处在4个Cl原子所组成的正方形的中心
C H2O是极性分子,分子中O原子不处在2个H原子所连成的直线的中央
D CO2是非极性分子,分子中C原子不处在2个O原子所连成的直线的中央
查看答案和解析>>
科目:高中化学 来源: 题型:
Zn-MnO2干电池应用广泛,其电解质溶液是ZnCl2-NH4Cl混合溶液。
 |
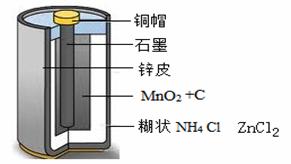
(1)该电池的负极材料是________。电池工作时,电子从Zn极流向______(填“正
极”或“负极”)。
(2)若ZnCl2-NH4Cl混合溶液中含有杂质Cu2+,会加速某电极的腐蚀,其主要原因
是 。欲除去Cu2+,最好选用下列试剂中的__________(填代号)。
A.NaOH B.Zn C.Fe D.NH3·H2O
(3)MnO2的生产方法之一是以石墨为电极,电解酸化的MnSO4溶液制取,请问MnO2
在 极产生。阴极的电极反应式是 。若电解电路中通过2 mol电子,MnO2的理论产量为__________g。(MnO2的摩尔质量为:87g/mol)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com