
���� ��1��̽���¶ȶԷ�Ӧ���ʵ�Ӱ�죬�����¶ȿɼӿ췴Ӧ���ʣ�
��2���ṩ�������ӿ췴Ӧ���ʣ������Ϊ���ԣ�
��3��ֻ��һ֧�Թ��м������Ȼ�����Һ������һ֧�Թ��γɶԱ����飬̽�������Ի�ѧ��Ӧ���ʵ�Ӱ�죻�����1mL��Һ���B�Թ���Һ����ϡ�ͣ�ʹŨ�ȷ����ı䣮
��� �⣺��1��A��B��֧�Թ��м���5mL5%H2O2��Һ��B�е��¶ȱ�A�ߣ����Թ�B�в������ݵ����ʿ죬˵�������¶ȿɼӿ�H2O2�ķֽ����ʣ�
�ʴ�Ϊ��B�������¶ȿɼӿ�H2O2�ķֽ����ʣ�
��2����ͬʱ���Թ�A��B�м���1mL1mol/L��FeCl3��Һ����Ϊ�������ӿ췴Ӧ���ʣ������Ϊ���ԣ�
�ʴ�Ϊ����ͬʱ���Թ�A��B�м���1mL1mol/L��FeCl3��Һ��
��3��ֻ��һ֧�Թ��м������Ȼ�����Һ������һ֧�Թ��γɶԱ����飬̽�������Ի�ѧ��Ӧ���ʵ�Ӱ�죻���˷�����Ʋ���������Ϊ�����1mL��Һ���B�Թ���Һ����ϡ�ͣ�ʹŨ�ȷ����ı䣬
�ʴ�Ϊ��̽�������Ի�ѧ��Ӧ���ʵ�Ӱ�죻���Թ�B�м���1mL��FeCl3��Һ��ʹH2O2��Ũ�Ƚ��ͣ�
���� ���⿼����̽��Ӱ�췴Ӧ���ʵ����أ�ʵ�鷽������ƣ��Ѷ�һ�㣬ע����������е�һ�����о�������ʹ�ã�Ϊ�״��㣮


 �¿α�����Ķ�ѵ��ϵ�д�
�¿α�����Ķ�ѵ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 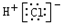 | |
| B�� | NH4Br�ĵ���ʽ��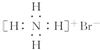 | |
| C�� | N2�Ľṹʽ�� | |
| D�� | ԭ�Ӻ�����18�����ӵ���ԭ�ӣ�3517Cl |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1��1 | B�� | 2��3 | C�� | 1��2 | D�� | 2��1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | CH2�TCH2+HCl$\stackrel{һ������}{��}$CH3CH2Cl | B�� | CH4+Cl2$\stackrel{����}{��}$CH3Cl+HCl | ||
| C�� | C2H4+3O2$\stackrel{��ȼ}{��}$2CO2+2H2O | D�� | 2CH3CH2OH+2Na��2CH3CH2ONa+H2�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | S��g��+O2��g���TSO2��l��|��H|��297.3 kJ•mol-1 | |
| B�� | 1molSO2�ļ����ܺʹ���1molS��1molO2����֮�� | |
| C�� | S��s��+O2��g���TSO2��g��|��H|��297.3 kJ•mol-1 | |
| D�� | 1molSO2�ļ����ܺ�С��1molS��1molO2����֮�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | C3H4�� H2 | B�� | C3H8�� CO | C�� | CH4�� C3H4 | D�� | C3H6�� CO2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
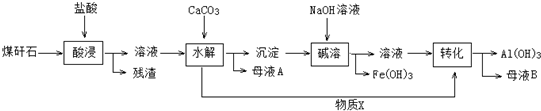
| ���� | ��ʼ����pH | ��ȫ����pH |
| Fe3+ | 2.1 | 3.2 |
| Al3+ | 4.1 | 5.4 |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com