
�����£��й�����������Һ��������ȷ����(������Һ��Ϻ������仯)(����)
| ��� | �� | �� | �� | �� |
| pH | 12 | 12 | 2 | 2 |
| ��Һ | ��ˮ | ����������Һ | ���� | ���� |
 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
������������ȷ����
| A����ͬ���ʵ���Ũ�ȵĢ�CH3COONa��Һ��NaNO3��Һ��NH4Cl��Һ��NaOH��Һ��pH�Ĵ�С˳���ǣ���>��>��>�� |
| B����Na2SO3��NaHSO3���Һ�У�c(Na+)+c(H+)=c(HSO3-)+c(OH-)+2c(SO32-) |
| C����ͬ�����£�pH=10��CH3COONa��Һ�Ͱ�ˮ�У���ˮ�������c(OH-)ǰ�ߴ��ں��� |
| D��ij��Һ��ֻ��Na+��CH3COO-��H+��OH-�������ӣ�����Һһ�����ּ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
25��ʱ��ˮ��Һ��c(H+)��c(OH��)�ı仯��ϵ��ͼ������a c��ʾ�������жϴ������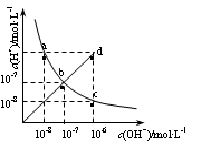
| A��a c�����ϵ�����һ�㶼��c(H+)��c(OH��)��10-14 |
| B��b d�߶�������һ���Ӧ����Һ�������� |
| C��d���Ӧ��Һ���¶ȸ���25�棬pH��7 |
| D��CH3COONa��Һ������λ��c�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
���и���������,����ǿ����ʵ���(����)
| A��HBr��HCl��BaSO4 |
| B��NH4Cl��CH3COOH��Na2S |
| C��NaOH��Ca(OH)2��NH3��H2O |
| D��HClO��NaF��Ba(OH)2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��֪CuSO4��Һ�ֱ���Na2CO3��Һ��Na2S��Һ�ķ�Ӧ������£�
(1)CuSO4��Na2CO3
��Ҫ��Cu2����CO32����H2O=Cu(OH)2����CO2��
��Ҫ��Cu2����CO32��=CuCO3��
(2)CuSO4��Na2S
��Ҫ��Cu2����S2��=CuS��
��Ҫ��Cu2����S2����2H2O=Cu(OH)2����H2S��
���м������ʵ��ܽ�ȴ�С�ıȽ��У���ȷ���� (����)
| A��CuS<Cu(OH)2<CuCO3 | B��CuS>Cu(OH)2>CuCO3 |
| C��Cu(OH)2>CuCO3>CuS | D��Cu(OH)2<CuCO3<CuS |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
25��ʱ��ˮ�д��ڵ���ƽ�⣺H2O H����OH�������й���ˮ��˵��������ȷ����(����)
H����OH�������й���ˮ��˵��������ȷ����(����)
| A��ˮ�ĵ��������ȹ��� |
| B����ˮ�м�������ϡ���ᣬc(H��)����KW���� |
| C����H������Һ�����ԣ���OH������Һ�Լ��� |
| D��ˮ�Ǽ����ĵ���ʣ���50��ʱˮ��pHС��7 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
25��ʱ��ijŨ�ȵ��Ȼ����Һ��pH��4�����������в���ȷ����(����)
| A����Һ�е�c(OH��)��1��10��10 mol��L��1 |
| B����Һ�е�c(Cl��)>c(NH4+)>c(H��)>c(OH��) |
| C����Һ�е�c(H��)��c(NH4+)��c(Cl��)��c(OH��) |
| D����Һ�е�c(NH3��H2O)��c(NH4+) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
ij�¶��£���pH��6������ˮ�м���NaHSO4���壬�����¶Ȳ��䣬�����Һ��pHΪ2�����жԸ���Һ�������У�����ȷ����(����)
| A�����¶ȸ���25��C |
| B����ˮ���������H����Ũ����1.0��10��10 mol/L |
| C������NaHSO4����������ˮ�ĵ��� |
| D�����¶��¼�������pH��12��NaOH��Һ��ʹ����Һǡ�ó����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
���е��뷽��ʽ����д��ȷ���� (����)
A��NH4+��H2O NH3��H2O��H�� NH3��H2O��H�� |
B��S2����2H2O H2S��2OH�� H2S��2OH�� |
C��CH3COOH��H2O CH3COO����H3O�� CH3COO����H3O�� |
D��CH3COOH��OH�� CH3COO����H2O CH3COO����H2O |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com