
某学生鉴定甲盐溶液的流程如图所示,下列说法正确的是
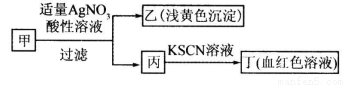
A.如果甲中含有S2-,则乙是硫磺沉淀
B.如果乙是AgCl沉淀,那么甲是FeCl3
C.丙中肯定含有Fe3+,所以甲是FeBr2
D.甲中含有铁元素,可能显示+2或者+3价
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2016届江西省高安市高三上学期第二次段考化学试卷(解析版) 题型:选择题
将Mg和Cu组成的混合物7.64 g投入足量的稀硝酸中使其完全反应,得到的唯一还原产物NO在标准状况下体积为2.24 L。将反应后的溶液稀释为1 L,测得溶液的pH=1,此时溶液中NO的浓度为
A.0.3 mol/L B.0.4 mol/L C.0.5 mol/L D.0.6 mol/L
查看答案和解析>>
科目:高中化学 来源:2016届广东省英德市高三上学期第二次月考理综化学试卷(解析版) 题型:选择题
下列表示对应化学反应的离子方程式.其中正确的是
A.向NaAlO2溶液中通入过量的CO2:2AlO2﹣+CO2+3H2O═2Al(OH)3↓+CO32﹣
B.NH4HCO3溶液中加入过量氢氧化钠溶液:NH4++OH﹣═ NH3·H2O
C.AlCl3溶液中滴加过量氨水:Al3+ + 3NH3·H2O ═ 3NH4++ Al(OH)3↓
D.磁性氧化铁(Fe3O4)溶于稀硝酸3Fe2++4H++NO3﹣═3Fe3++NO↑+2H2O
查看答案和解析>>
科目:高中化学 来源:2016届重庆市高三上学期期中测试理综化学试卷(解析版) 题型:选择题
一定量的浓硝酸与足量铜完全反应,得到硝酸铜溶液和NO2、NO的混合气体2.24L(标准状况),这些气体与一定体积O2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸。若向所得硝酸铜溶液中加入4 mol·L-1NaOH溶液至Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是50 mL,下列说法正确的是
A.参加反应的硝酸是0.4 mol
B.消耗氧气的体积为1.68 L
C.混合气体中含NO2 1.12 L
D.此反应过程中转移的电子为0.3 mol
查看答案和解析>>
科目:高中化学 来源:2016届山东省高三上学期第一次诊断测试化学试卷(解析版) 题型:简答题
氧化还原反应是化学反应中的基本反应之一,研究氧化还原反应,对人类的进步具有极其重要的意义。
(1)已知:2BrO3-+C12=Br2+2C1O3- ; 5C12+I2+6H2O=2HIO3+10HC1;
C1O3-+5C1-+6H+=3C12+3H2O
则C1O3-、BrO3-、IO3-、C12的氧化性由弱到强的排序为
(2)已知Fe3+的氧化性强于I2,请你从所给试剂中选择所需试剂,设计一个实验加以证明。(提示:请写出实验步骤、现象及结论)①FeCl3溶液 ②碘水 ③KI溶液 ④稀H2SO4 ⑤淀粉溶液
(3)二十世纪初期,化学家合成出极易溶于水的NaBH4。在强碱性条件下,常用NaBH4处理含Au3+的废液生成单质Au,已知,反应后硼元素以BO2-形式存在,反应前后硼元素化合价不变,且无气体生成,则发生反应的离子方程式为
(4)某强氧化剂[RO(OH)2]+ 能将Na2SO3氧化。已知含2.0×10-3 mol [RO(OH)2]+ 离子的溶液,恰好跟25.0 mL 0.2 mol/L 的Na2SO3溶液完全反应,则反应后R的化合价为 价。
(5)将32 g 铜与140 mL一定浓度的硝酸反应,铜完全溶解产生的NO和NO2混合气体在标准状况下的体积为11.2 L。请回答:
①待产生的气体全部释放后,向溶液加入V mL amol·L-1的NaOH溶液,恰好使溶液中的Cu2+全部转化成沉淀,则原硝酸溶液的浓度为 mol/L。(用含V、a的式子表示)
①欲使铜与硝酸反应生成的气体在NaOH溶液中全部转化为NaNO3,至少需要H202的质量为 g。
查看答案和解析>>
科目:高中化学 来源:2016届浙江省新安江校区高三上学期第二次模拟化学试卷(解析版) 题型:选择题
某溶液中含有NH4+、SO32-、SiO32-、Br - CO32-、Na+,向该溶液中通入过量的Cl2,下列判断正确的是
①反应前后,溶液中离子浓度基本保持不变的有NH4+、Na+ ②有胶状物质生成
③有气体产生 ④溶液颜色发生变化 ⑤溶液中共发生了2个氧化还原反应
A.①②③④ B.①②③④⑤ C.①③④⑤ D.②④⑤
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北省高一上期中测试化学试卷(解析版) 题型:选择题
下列反应属于氧化还原反应的是
A.CaCO3+2HCl=CaCl2+CO2↑ + H2O B.CaO+H2O=Ca(OH)2
C.2H2O2 2H2O+O2↑ D.CaCO3
2H2O+O2↑ D.CaCO3 CaO+CO2↑
CaO+CO2↑
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广东省清远市高二上学期10月月考化学试卷(解析版) 题型:填空题
为实现 “节能减排” 和“低碳经济”的一项课题是如何将CO2转化为可利用资源。目前,工业上常用CO2来生产燃料甲醇。现进行如下实验:在体积为l L的密闭恒容容器中,充入l mol CO2和3mol H2,一定条件下发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH=-49.0 kJ/mol。测得CO2和CH3OH(g)的浓度随时间变化如图所示。
CH3OH(g)+H2O(g) ΔH=-49.0 kJ/mol。测得CO2和CH3OH(g)的浓度随时间变化如图所示。

(1)该反应的平衡常数表达式K= ;
(2)从反应开始到平衡时,CH3OH的平均反应速率v(CH3OH)= (注明单位);H2的转化率= ;
(3)下列说法中,能说明上述反应达到平衡状态的是
A.每消耗1mol CO2的同时生成1mol CH3OH
B.CO2、H2、CH3OH和H2O的物质的量的比为1:3:1:1
C.容器中气体的压强不再改变
D.容器中气体的密度不再改变
(4)下列措施中,能使上述平衡状态向正反应方向移动的是
A.升高温度
B.将CH3OH(g)从体系中分离
C.使用高效催化剂
D.恒温恒容再充入1 molCO2和3 mol H2
查看答案和解析>>
科目:高中化学 来源:2016届河南省英文学校高三上学期期中测试化学试卷(解析版) 题型:选择题
有Fe2+、NO3—、Fe3+、NH4+、H+和H2O六种粒子,属于同一氧化还原反应中的反应物和生成物,下列叙述不正确的是
A.氧化剂和还原剂的物质的量之比为1:8
B.每1molNO3—发生氧化反应,转移8mol e-
C.该过程说明Fe(NO3)2溶液不宜加酸酸化
D.若把该反应设计为原电池,则负极反应为Fe2+—e–=Fe3+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com