
下列关于实验原理或操作的叙述中,不正确的是:
A. 从碘水中提取单质碘时,不能用无水乙醇代替CCl4
B. 可用新制的Cu(OH)2悬浊液检验牙膏中存在的甘油
C. 纸层析实验中,须将滤纸上的试样点浸入展开剂中
D. 实验室中提纯混有少量乙酸的乙醇,可采用先加生石灰,过滤后再蒸馏的方法
【解析】本题是一组实验操作或原理的正误判断问题。实验操作的正误,实际根源还是实验原理。A、乙醇和碘与水均互溶,不能作为萃取剂使用。考查萃取原理。B、新制Cu(OH)2悬浊液用来检验醛基而不是羟基。C、纸层析实验中,不能将滤纸上的试样点浸入展开剂中,否则式样会溶解在展开剂中。D、除乙酸用碱性氧化物,氧化钙还能吸水,过滤后利用乙醇沸点低的原理进行蒸馏最好。
教与学提示:
本题涉及的化学实验都是重要的经典的。化学实验的教学中要重视重点实验的操作与原理,更要重视正确与错误的操作存在的与原理的矛盾。符合高中生理解记忆的特点,多想想为什么,才能顺利又高效掌握化学实验。实验教学还有:仪器链接、实验改进、数据处理、药品与仪器选择、药品添加顺序与药品用量、实验创新等内容。
【答案】C


科目:高中化学 来源: 题型:
A、B、C、D均为含苯环的有机物,且相对分子质量B>A>C。已知有机物A的结构简式为
(1)有机物A既能与NaOH溶液反应,又能与NaHCO3溶液反应,写出A和NaHCO3溶液反应的化学方程式: 。
(2)①有机物B在浓H2SO4存在的条件下相互作用生成一种环状酯如图,则有机物B的结构简式为 。②等物质的量的B分别与Na、NaOH、NaHCO3充分反应,消耗Na、NaOH、NaHCO3的物质的量之比为 。
(3)1mol A、C完全燃烧,消耗O2的质量相等,且1mol C能与1mol Na完全反应,则C的结构简式为 。
(4)D与B互为同分异构体,且知其苯环上连有三个取代基,苯环上的一氯代物只有2种,D不与NaHCO3溶液 反应,能与Na反应也能与NaOH溶液反应,等质量的D消耗Na、NaOH物质的量之比为2 :3,则D的结构简式为(只写二种) 。
查看答案和解析>>
科目:高中化学 来源: 题型:
以NA表示阿伏加德罗常数,下列说法正确的是
A.0.1 mol Fe与足量盐酸反应,转移的电子数为0.3 NA
B.28 g CO中所含的原子数为2 NA
C.0.1 mol·L-1 Na2CO3溶液中,含有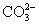 数为0.1 NA
数为0.1 NA
D.标准状况下,22.4 L苯的分子数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
拟用右图所示装置制取四种干燥、纯净的气体(图中加热装置和气体的收集装置均已略去;必要时可以加热;a、b、c、d表示相应仪器中加入的试剂)。其中不能达到目的的是

| 选项 | 制取气体 | a | b | c | d |
| A | NO | 稀硝酸 | 铜片 | H2O | 浓硫酸 |
| B | O2 | 双氧水 | MnO2 | H2O | 浓硫酸 |
| C | NH3 | 浓氨水 | 碱石灰 | 浓硫酸 | H2O |
| D | SO2 | 浓盐酸 | Na2SO3粉末 | NaHSO3溶液 | 浓硫酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
CuSO4·5H2O是铜的重要化合物,有着广泛的应用。以下是CuSO4·5H2O的实验室制备流程图。
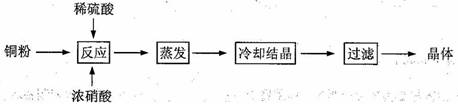
根据题意完成下列填空:
(1)向含铜粉的稀硫酸中滴加浓硝酸,在铜粉溶解时可以观察到的实验现象: 、
。
(2)如果铜粉、硫酸及硝酸都比较纯净,则制得的CuSO4·5H2O中可能存在的杂质是 ,除去这种杂质的实验操作称为 。
(3)已知:CuSO4+2NaOH=Cu(OH)2↓+ Na2SO4
称取0.1000 g提纯后的CuSO4·5H2O试样于锥形瓶中,加入0.1000 mol/L氢氧化钠溶液28.00 mL,反应完全后,过量的氢氧化钠用0.1000 mol/L盐酸滴定至终点,耗用盐酸20.16 mL,则0.1000 g该试样中含CuSO4·5H2O g。
(4)上述滴定中,滴定管在注入盐酸之前,先用蒸馏水洗净,再用 。
在滴定中,准确读数应该是滴定管上蓝线 所对应的刻度。
(5)如果采用重量法测定CuSO4·5H2O的含量,完成下列步骤:
① ②加水溶解③加氯化钡溶液,沉淀④过滤(其余步骤省略)
在过滤前,需要检验是否沉淀完全,其操作是
(6)如果1.040 g提纯后的试样中含CuSO4·5H2O的准确值为1.0 15 g,而实验测定结果是l.000 g 测定的相对误差为 。
15 g,而实验测定结果是l.000 g 测定的相对误差为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
有A、B、C、D、E和F六瓶无色溶液,他们都是中学化学中常用的无机试剂。纯E为无色油状液体;B、C、D和F是盐溶液,且他们的阴离子均不同。现进行如下实验:
①A有刺激性气味,用沾有浓盐酸的玻璃棒接近A时产生白色烟雾;
②将A分别加入其它五中溶液中,只有D、F中有沉淀产生;继续加入过量A时,D中沉淀无变化,F中沉淀完全溶解;
③将B分别加入C、D、E、F中,C、D、F中产生沉淀,E中有无色、无味气体逸出;
④将C分别加入D、E、F中,均有沉淀生成,再加入稀HNO3,沉淀均不溶。
根据上述实验信息,请回答下列问题:
(1) 能确定溶液是(写出溶液标号与相应溶质的化学式):
(2) 不能确定的溶液,写出其标号、溶质可能的化学式及进一步鉴别的方法:
查看答案和解析>>
科目:高中化学 来源: 题型:
洗车安全气囊是德国安 全的重要保障。当车辆发生碰撞的瞬间,安全装置通电点火使其中的粉末分解释放出大量的氮气形成气囊,从而保护司机及乘客免受伤害。为研究安全气囊工作的化学原理,取安全装置中的粉末进行实验。经组成分析,确定该粉末仅Na、Fe、N、O四种元素。水溶性试验表明,固体粉末部分溶解。经检测,可溶物为化合物甲;不溶物为红棕色固体,可溶于盐酸。
全的重要保障。当车辆发生碰撞的瞬间,安全装置通电点火使其中的粉末分解释放出大量的氮气形成气囊,从而保护司机及乘客免受伤害。为研究安全气囊工作的化学原理,取安全装置中的粉末进行实验。经组成分析,确定该粉末仅Na、Fe、N、O四种元素。水溶性试验表明,固体粉末部分溶解。经检测,可溶物为化合物甲;不溶物为红棕色固体,可溶于盐酸。
取13.0g化合物甲,加热使其完全分解,生成氮气和单质乙,生成的氮气折合成标准状况下的体积为6.72L。单质乙在高温隔绝空气的条件下与不溶物红棕色粉末反应生成化合物丙和另和一种单质。化合物丙与空气接触可转化为可溶性盐。
请回答下列问题:
(1)甲的化学式为 ,丙的电子式为 。
(2)若丙在空气中转化为碳酸氢盐,则反应的化学方程式为 。
(3)单质乙与红棕色粉末发生反应的化学方程式为 ,安全气囊中红棕色粉末的作用是 。
(4)以下物质中,有可能作为安全气囊中红棕色粉末替代品的是 。
A. KCl B. KNO3 C. Na2S D. CuO
(5)设计一个实验方案,探究化合物丙与空气接触后生成可溶性盐的成分(不考虑结晶水合物) 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验设计和结论相符的是( )
A.将碘水倒入分液漏斗,加适量乙醇,振荡后静置,可将碘萃取到乙醇中
B.某气体能使湿润的红色石蕊试纸变蓝,该气体水溶液一定显碱性
C.某无色溶液中加Ba(NO3)2溶液,再加稀盐酸,沉淀不溶解,则原溶液中一定有SO42-
D.在含FeCl2杂质的FeCl3溶液中通足量Cl2后,充分加热,除去过量的Cl2,即可得到较纯净的FeCl3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
酯是重要的有机合成中间体,广泛应用于溶剂、增塑剂、香料、粘合剂及印刷、纺织等工业。乙酸乙酯的实验室和工业制法常采用如下反应:
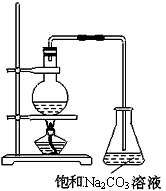
CH3COOH+C2H5OH 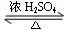 CH3COOC2H5+H2O
CH3COOC2H5+H2O
请根据要求回答下列问题:
(1)欲提高乙酸的转化率,可采取的措施有 、 等。
(2)若用上图所示装置来制备少量的乙酸乙酯,产率往往偏低,其原因可能为 、
等。
(3)此反应以浓硫酸为催化剂,可能会造成 、 等问题。
(4)目前对该反应的催化剂进行了新的探索,初步表明质子酸离子液体可用作此反应的催化剂,且能重复使用。实验数据如下表所示(乙酸和乙醇以等物质的量混合)
| 同一反应时间 | 同一反应温度 | ||||
| 反应温度/℃ | 转化率(%) | 选择性(%)* | 反应时间/h | 转化率(%) |
|
| 40 | 77.8 | 100 | 2 | 80.2 | 100 |
| 60 | 92.3 | 100 | 3 | 87.8 | 100 |
| 80 | 92.6 | 100 | 4 | 92.3 | 100 |
| 120 | 94.5 | 98.7 | 6 | 93.0 | 100 |
| *选择性100%表示反应生成的产物是乙酸乙酯和水 |
①根据表中数据,下列 (填字母)为该反应的最佳条件。
A.120℃,4h B.80℃,2h C.60℃,4h D.40℃,3h
② 当反应温度达到120℃时,反应选择性降低的原因可能为 _____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com