
【题目】下列离子方程式正确的是
A. 铁与稀盐酸反应:2Fe+6H+===2Fe3++3H2↑
B. 在过氧化钠中加入稀硫酸:O22- +4H+===2H2O+O2↑
C. 氢氧化钡溶液与稀硫酸反应:Ba2++SO42-===BaSO4↓
D. 澄清石灰水与过量的小苏打溶液反应:Ca2++2OH-+2HCO![]() ===CaCO3↓+2H2O+ CO32-
===CaCO3↓+2H2O+ CO32-
 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案科目:高中化学 来源: 题型:
【题目】用气体传感器可以检测汽车尾气中CO的含量。传感器是以燃料电池为工作原理,其装置如右图所示,该电池中电解质为氧化钇—氧化钠,其中O2-可以在固体介质NASICON中自由移动。下列说法错误的是

A.负极的电极反应式为:CO+O2-![]() 2e-=CO2
2e-=CO2
B.工作时电子由电极a通过传感器流向电极b
C.工作时电极b作正极,O2-由电极a流向电极b
D.传感器中通过的电流越大,尾气中CO的含量越高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生产、生活、社会密切相关。下列有关说法正确的是
A. 点燃爆竹后,硫燃烧生成SO3
B. 中国古代利用明矾溶液的酸性清除铜镜表明的铜锈
C. 服用阿司匹林出现水杨酸反应时,用NaOH溶液解毒
D. 使用含钙离子浓度较大的地下水洗衣服,肥皂去污能力增强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于可逆反应4 NH3(g)+5O2(g)![]() 4NO(g)+6 H2O(g),下列叙述正确的是
4NO(g)+6 H2O(g),下列叙述正确的是
A. NH3和H2O化学反应速率关系是2v正(NH3)= 3v正(H2O)
B. 达到化学平衡时,4v正(O2)= 5v逆(NO )
C. 达到化学平衡时,若增加容器体积,则正反应速率减少,逆反应速率增大
D. 若单位时间内生成x mol NO的同时,消耗x mol NH3 ,则反应达到平衡状态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝分别与足量的稀盐酸和氢氧化钠溶液反应时,当两个反应放出的气体在相同状况下体积相等时,反应中消耗的盐酸和氢氧化钠的物质的量之比为( )
A. 1∶1 B. 2∶1 C. 3∶1 D. 1∶3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【化学——选修3:物质结构与性质】已知 A、B、C、D是原子序数依次增大的四种短周期主族元素,A的周期数等于其主族序数, B原子的价电子排布为nsnnpn,D是地壳中含量最多的元素。E是第四周期的p区元素且最外层只有2对成对电子,F元素的基态原子第四能层只有一个电子,其它能层均已充满电子。

(1)基态E原子的价电子排布图_______________。
(2)B、C、D三元素第一电离能由大到小的顺序为(用元素符号表示)______________。
(3)BD32-中心原子杂化轨道的类型为________杂化;CA4+的空间构型为__________(用文字描述)。
(4)1mol BC-中含有π键的数目为______NA。
(5)D、E元素最简单氢化物的稳定性 > (填化学式),理由是 。
(6)C、F两元素形成的某化合物的晶胞结构如右图所示,则该化合物的化学式是 ,C原子的配位数是 。若相邻C原子和F原子间的距离为anm,阿伏伽德罗常数为NA,则该晶体的密度为_____________g/cm3(用含a、NA的符号表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2015年,我国科学家屠呦呦因发现青蒿素而荣获诺贝尔奖。由植物黄花蒿叶中提取的青蒿素还可合成用于抗氯喹恶性疟及凶险型疟疾的蒿甲醚,器合成路线如下:
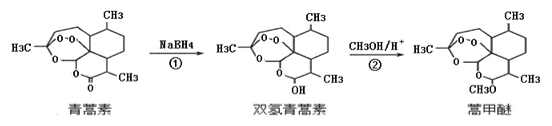
下列说法不正确的是()
A. 青蒿素的分子式是C15H22O5,属于烃的衍生物
B. 双氢青蒿素中含有过氧键,遇湿润的淀粉碘化钾试纸立刻显蓝色
C. 蒿甲醚可以犮生水解反应
D. 反应②为取代反应,有H2O生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下图装置进行下列实验:将①中溶液滴入②中,预测的现象与实际相符的是

选项 | ①中物质 | ②中物质 | 预测②中的现象 |
A | 稀盐酸 | 碳酸钠与氢氧化钠的混合溶液 | 立即产生气泡 |
B | 浓硝酸 | 用砂纸打磨过的铝条 | 产生红棕色气体 |
C | 草酸溶液 | 高锰酸钾酸性溶液 | 溶液逐渐褪色 |
D | 液溴 | 苯 | 生成白雾 |
A. A B. B C. C D. D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com