
��X��Y��Z���ֶ�����Ԫ�أ�X����̬�⻯�ﻯѧʽΪH2X�����⻯��ķ�������X���������ķ�����֮��Ϊ17��40��Xԭ�Ӻ�������������������ȣ�Y��X�����γ����ӻ�����Y2X��Y�������ӵ��Ӳ�ṹ��Ne��ͬ��Z��Xͬ���ڣ�����̬������˫ԭ�ӷ��ӣ���ԭ�ӹ���1�Ե��ӡ��Իش�
��1��д����Ԫ�ط��ţ�X ��Y ��Z ��
��2��X���ӵĽṹʾ��ͼΪ ��X��Y�γɵ����ӻ�����ĵ���ʽΪ �� Z�����γɵĻ�����ĵ���ʽΪ ��
��3��Y�����ڿ�����ȼ�յĻ�ѧ����ʽΪ ����������ˮ��Ӧ�Ļ�ѧ����ʽΪ ��

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���ƺ��ʵ�����������Ӧ2Fe3++2I-  2Fe2+I2��Ƴ�����ͼ��ʾ��ԭ��ء�����˵������ȷ����
2Fe2+I2��Ƴ�����ͼ��ʾ��ԭ��ء�����˵������ȷ����
A�������е�K+����FeCl3��Һ
B����Ӧ��ʼʱ������ʯī�缫�Ϸ���������Ӧ
C�������ƶ���Ϊ��ʱ����Ӧ�ﵽ��ѧƽ��״̬
D�������ƶ���Ϊ����ڼ�������FeCl2���壬����ʯī�缫Ϊ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����й����ʽṹ��˵����ȷ����
A��78 g Na2O2�������������������Ӹ�����Ϊ4NA
B��3.4 g�������0.6NA��N��H��
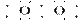 C��Na2O2�ĵ���ʽΪ: Na Na
C��Na2O2�ĵ���ʽΪ: Na Na
D��PCl3��BCl3����������ԭ�ӵ�����㶼�ﵽ8�����ȶ��ṹ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
X��Y��ZΪ���ֶ�����Ԫ�أ�X��Y�������ڵ��������ڣ�Xԭ�ӵ�������������Yԭ��������������2����Y��ԭ��������X��ԭ��������5��Zԭ����Yԭ�ӵ�����������֮��Ϊ3������������ȷ����
A. X��Y��Z����Ԫ�ز������һ����
B. X������Z����ֱ�ӷ�Ӧ���������ֻ�����
C. X��Y��Z������������Ӧ��ˮ����������ᡢ������Ե�����
D. X��Y�γɵ�һ�����Ӹ�H����Ӧ������Y������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�ڶ�����Ԫ����,ԭ��������Ӳ�ֻ��1����2�����ӵ�Ԫ���ǣ�����
A.����Ԫ��
B.ϡ������Ԫ��
C.�ǽ���Ԫ��
D.��ȷ��Ϊ��һ��Ԫ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�Ž��з�������Ԫ�����ڱ�ʱ������Ԫ����δ���֣�����Ϊ�������ڵ�����Ԫ�������˿�λ���������ǵ�һЩ��������Ԥ�⣬X�����е�һ�֡���衱Ԫ�أ��������¹���ѧ���Ŀ��շ��֣���֤ʵ�Ž��з�ʱ��Ԥ���൱ȷ������Ԫ�������ɣ������й�X�����ʵ���������ȷ���ǣ�����
A��X��������ˮ��Ӧ B��X�γɵ�����������ˮ��Ӧ������
C��X���γ�������XO D��XH4���ȶ��Ա�SiH4�ĵ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
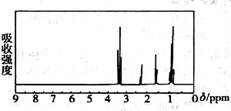
��ͼ��һ����˴Ź����ף�����۲�ͼ�ף���������������������� �� ��
A��CH3CH2CH2CH3 B��(CH3)2CHCH3 C��CH3CH2CH2OH D��CH3CH2COOH
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��.��֪��4Al(s)+3O2(g) = 2Al2O3(s) ��H=��2834.9KJ•mol��1
Fe2O3(s)+ C(s)=
C(s)= CO2(g)+2Fe(s) ��H=+234.1KJ•mol��1
CO2(g)+2Fe(s) ��H=+234.1KJ•mol��1
C(s)+O2(g)= CO2(g) ��H=��393.5KJ•mol��1
д�������������������ȷ�Ӧ���Ȼ�ѧ����ʽ______________ ��
��.��2L�ܱ������ڣ�800��ʱ��Ӧ��2NO(g)+O2(g)  2NO2(g) ��H��0 ��ϵ�У�n(NO)��ʱ��ı仯�����
2NO2(g) ��H��0 ��ϵ�У�n(NO)��ʱ��ı仯�����
| ʱ�䣨s�� | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(1) д���÷�Ӧ��ƽ�ⳣ������ʽ��K= �� ��O2��ʾ��0~2s�ڸ÷�Ӧ��ƽ�����ʦͣ�O2��= ��
(2) �����о�Ŀ�ĺ�ʾ��ͼ������� ��
| A | B | C | D | |
| �о�Ŀ�� | ѹǿ�Է�Ӧ��Ӱ�죨P1>P2�� | �¶ȶԷ�Ӧ��Ӱ�� | ƽ����ϵ����O2�Է�Ӧ��Ӱ�� | �����Է�Ӧ��Ӱ�� |
| ͼʾ |
|
|
|
|
III.��ѧ�������һ��ʹ�ù������ʵĸ�Чȼ�ϵ�ء�һ���缫ͨ���������һ���缫ͨ��ȼ�����������й��������Dz�����Y2O3 ��ZrO2���壬���ڸ������ܴ���O2�����ӣ�����������Ӧ������ȫ�����Ա��飨C3H8������ȼ�ϡ�
(1)����صĸ�����ӦʽΪ________________��
(2)���ŵ�ʱ�����������O2��������____���ƶ����������������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com