
【题目】下列关于溶液和胶体的叙述,一定正确的是( )。
A. 溶液是电中性的,胶体是带电的
B. 卤水点豆腐与胶体的性质无关
C. 布朗运动是胶体微粒特有的运动方式,可以据此把胶体和溶液、悬浊液区别开来
D. 一束光线分别通过溶液和胶体时,后者会出现明显的光路,前者则没有
 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案科目:高中化学 来源: 题型:
【题目】下列各组离子能在溶液中大量共存的是
A. Ag+、K+、NO3-、C1- B. Mg2+、Na+、Cl-、SO42-
C. NH4+、Cu2+、OH-、Cl- D. H+、Na+、HCO3-、SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定量CO2与足量C在体积可变的恒压密闭容器中发生反应:C(s)+CO2(g) ![]() 2CO(g),平衡时体系中气体体积分数与温度的关系如下图所示:
2CO(g),平衡时体系中气体体积分数与温度的关系如下图所示:

下列说法不正确的是
A. 550℃时,v逆小于925℃时v逆
B. 650℃时,反应达平衡后,CO2的转化率为25%
C. 由图中数据分析可得,该反应为放热反应
D. T℃时,若向平衡体系内充入惰性气体,化学平衡将向正反应方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子,在水溶液中能大量共存的是( )
A.Ba2+、Cl-、SO42-、Na+B.SO32-、CO32-、NH4+、H+
C.H+、K+、OH-、NO3-D.K+、Na+、Cl-、NO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于细胞中化学元素的叙述,错误的是
A. 细胞中的化学元素在无机自然界都能够找到
B. 占细胞鲜重和干重百分比最高的元素分别是O和C
C. 微量元素在细胞中含量很少,不是细胞生命活动必需的元素
D. C, K, Mg都是组成细胞的大量元素,C在各种有机物中都存在
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列描述中正确的是( )。
A.原子晶体中只含共价键
B.离子晶体中只含离子键,不含有共价键
C.分子晶体中只存在分子间作用力,不含其它化学键
D.任何晶体中,若含阳离子也一定还有阴离子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏加德罗常数的值,下列说法正确的是
A. 标准状况下,22.4L H2S和SO2的混合气体中含有的分子总数为NA
B. 1L1molL-1 FeCl3溶液完全水解产生的Fe(OH)3胶体粒子数为NA
C. 高温下,16.8gFe与足量的水蒸气完全反应失去的电子数为0.8NA
D. 28.6gNa2CO310H2O溶于水配成1L溶液,该溶液中阴离子数目为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝土矿的主要成分是Al2O3,含有杂质SiO2、Fe2O3、MgO。工业上从铝土矿中提取铝可采用如下工艺流程:
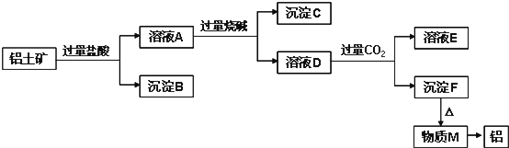
请回答下列问题:
(1)溶液A转化为溶液D发生的离子方程式为____________________;
(2)由物质M制取铝的化学方程式为____________________;
(3)溶液D中通入过量CO2生成沉淀F的离子方程式为____________________;
(4)取一定量的沉淀C置于试管中,逐滴向试管中加入过量HI至沉淀全部溶解,所得溶液中Fe元素以_______存在,检验该离子的实验操作和现象是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢化钠(NaH)是一种白色的离子化合物,其中钠元素是+1价;氢化钠与水反应放出氢气.下列叙述中不正确的是( )
A.NaH的电子式为 ![]()
B.NaH与H2O反应时水作氧化剂
C.NaH中氢元素的离子半径小于Li+的离子半径
D.H+与H﹣的核外电子排布不相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com