
【题目】一定量CO2与足量C在体积可变的恒压密闭容器中发生反应:C(s)+CO2(g) ![]() 2CO(g),平衡时体系中气体体积分数与温度的关系如下图所示:
2CO(g),平衡时体系中气体体积分数与温度的关系如下图所示:

下列说法不正确的是
A. 550℃时,v逆小于925℃时v逆
B. 650℃时,反应达平衡后,CO2的转化率为25%
C. 由图中数据分析可得,该反应为放热反应
D. T℃时,若向平衡体系内充入惰性气体,化学平衡将向正反应方向移动
 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案科目:高中化学 来源: 题型:
【题目】一定温度下,在三个体积约为1.0L的恒容密闭容器中发生反应:2CH3OH(g)CH3OCH3(g)+H2O(g)
容器编号 | 温度(℃) | 起始物质的量(mol) | 平衡物质的量(mol) | |
CH3OH(g) | CH3OCH3(g) | H2O(g) | ||
I | 387 | 0.20 | 0.080 | 0.080 |
Ⅱ | 387 | 0.40 | ||
Ⅲ | 207 | 0.20 | 0.090 | 0.090 |
下列说法正确的是( )
A.该反应的正方应为吸热反应
B.若起始时向容器I中充入CH3OH 0.1mol、CH3OCH3 0.15mol和H2O 0.10mol,则反应将向正反应方向进行
C.容器I中反应达到平衡所需时间比容器Ⅲ中的长
D.达到平衡时,容器I中的CH3OH体积分数比容器Ⅱ中的小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质互为同分异构体的一组是 ( )
A. 35Cl和37Cl B. H2O和H2O2
C. O2和O3 D. CH3CH2OH和CH3OCH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Fenton试剂常用于氧化降解有机污染物X。在一定条件下,反应初始时c(X)=2.0×10-3mol·L-1,反应10 min进行测定,得图1和图2。下列说法不正确的是
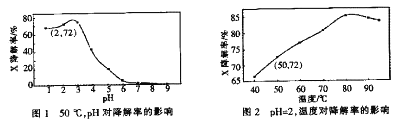
A. 50oC,PH在3~6之间,X降解率随pH增大而减小
B. pH=2,温度在40~80oC,X降解率随温度升高而增大
C. 无需再进行后续实验,就可以判断最佳反应条件是:PH=3、温度为80oC
D. pH=2、温度为50oC,10min内v(X)=1.44x10-4mol·L-1min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用氟硼酸(HBF4,属于强酸)代替硫酸作铅蓄电池的电解质溶液,可使铅蓄电池在低温下工作时的性能更优良,反应方程式为:Pb+PbO2+4HBF4![]() 2Pb(BF4)2+2H2O,Pb(BF4)2为可溶于水的强电解质,下列说法正确的是
2Pb(BF4)2+2H2O,Pb(BF4)2为可溶于水的强电解质,下列说法正确的是
A. 放电时,负极反应为:PbO2+4HBF4-2e-=Pb(BF4)2+2BF4-+2H2O
B. 充电时,当正极质量减少23.9g时转移0.2mol电子
C. 放电时,PbO2电极附近溶液的pH增大
D. 充电时,Pb电极的电极反应式为PbO2+4H++2e-=Pb2++2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某无色溶液甲中仅含有下列离子的几种( 不考虑水的电离以及离子的水解);
阳离子 | K+、Al3+、Fe3+、Ba2+、NH4+ |
阴离子 | Cl-、CO32-、HCO3-、SO42- |
取100mL溶液甲并分成两等份进行如下实验(假设每步完全反应):
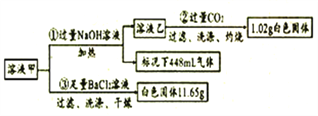
(1)由①可知,原溶液存在的离子有____,浓度为_____mol/L。
(2)写出实验②中生成沉淀的离子方程式_________。
(3)通入过量CO2充分反应后,需将反应后的混合溶液加热再过滤,其目的是_______。
(4)某同学通过分析认为该溶液中一定存在K+,其理由是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化硫酰(SO2C12)主要用作氯化剂。它是一种无色液体,熔点-54.1℃,沸点69.1℃。氯化硫酰可用干燥的二氧化硫和氯气在活性炭催化剂存在下反应制取:SO2(g)+C12(g)![]() SO2C12 (l) △H=-97.3kJ/mol
SO2C12 (l) △H=-97.3kJ/mol
(1)试写出常温常压下化学平衡常数K的表达式:K=____________;若在此条件下,将化学平衡常数K增大,化学反应速率V正也增大,可采取的措施是____________(选填编号)。
a.降低温度 b.移走SO2C12
c.增加反应物浓度 d.以上都不对
(2)为了提高上述反应中Cl2的平衡转化率,下列措施合理的是___________(选选填编号)。
a.缩小容器体积 b.使用催化剂
c.增加SO2浓度 d.升高温度
(3)在100℃时,往上述平衡体系中加入37C12,—段时间后,则平衡体系中含有37C1的物质有_______(选选填编号)。
a.只有37C12 b.只有 SO237Cl2 c. 37C12和SO237Cl2 d.无法判断
(4)下列描述中能说明上述反应己达平衡的是_____________ (选填编号)。
a.v (Cl2) =v (SO2)
b.容器中气体压强不随时间而变化
c.c (Cl2) : c (SO2) =1 : 1
d.容器中气体颜色不随时间而变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于溶液和胶体的叙述,一定正确的是( )。
A. 溶液是电中性的,胶体是带电的
B. 卤水点豆腐与胶体的性质无关
C. 布朗运动是胶体微粒特有的运动方式,可以据此把胶体和溶液、悬浊液区别开来
D. 一束光线分别通过溶液和胶体时,后者会出现明显的光路,前者则没有
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)科学家发现某药物M能治疗血管疾病,是因为它在人体内能释放出一种“信使分子”D。已知M的相对分子质量为227,由C、H、O、N四种元素组成,C、H、N的质量分数依次为15.86%、2.20%和18.50%,则M的分子式是______。D是双原子分子,相对分子质量为30,则D的分子式为_____。
(2)油脂A经下列途径可得到M:
![]()
图中②的提示:R—OH+HO—NO2![]() R—O—NO2+H2O(R代表烃基)
R—O—NO2+H2O(R代表烃基)
反应②的化学方程式为____________。
(3)C是B与乙酸在一定条件下反应生成的化合物,相对分子质量为134,写出C所有可能的结构简式:_________________。
(4)若将0.1 mol B与足量的金属钠反应,则需消耗_____ g金属钠。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com