
����Ŀ����¯���������з�������Ҫ��ӦΪ��![]() ����֪�÷�Ӧ�ڲ�ͬ�¶��µ�ƽ�ⳣ�����£�
����֪�÷�Ӧ�ڲ�ͬ�¶��µ�ƽ�ⳣ�����£�
�¶�/�� | 1000 | 1150 | 1300 |
ƽ�ⳣ�� | 4.0 | 3.7 | 3.5 |
��ش��������⣺
��1���÷�Ӧ��ƽ�ⳣ������ʽ![]() ______���÷�Ӧ������Ӧ��______��Ӧ������ȡ��������ȡ�����
______���÷�Ӧ������Ӧ��______��Ӧ������ȡ��������ȡ�����
��2����һ���ݻ�Ϊ10L���ܱ������У�1000��ʱ����Fe��Fe2O3��CO��CO2��1.0mol����Ӧ����10 min��ﵽƽ�⡣���ʱ�䷶Χ�ڷ�Ӧ��ƽ����Ӧ����![]() ______��CO��ƽ��ת����
______��CO��ƽ��ת����![]() ______��
______��
��3������ߣ�2����CO��ƽ��ת���ʣ��ɲ�ȡ�Ĵ�ʩ��______��
a.����Fe���� b.����Fe2O3���� c.�Ƴ�����CO2 d.��߷�Ӧ�¶�e.��С�������ݻ� f.������ʵĴ���
��4������������������![]() �ķ�ˮ�����У�Һ���ڼ��������¿��Խ��軯�������������Σ��䶾�Խ�Ϊ�軯���ǧ��֮һ���������ν�һ��������Ϊ�����ʡ�
�ķ�ˮ�����У�Һ���ڼ��������¿��Խ��軯�������������Σ��䶾�Խ�Ϊ�軯���ǧ��֮һ���������ν�һ��������Ϊ�����ʡ�
��ij����ˮ�к�KCN����Ũ��Ϊ650mg/L���������������������������·�Ӧ������N��Ϊ![]() �ۣ���
�ۣ���![]() ��������Ԫ����______��
��������Ԫ����______��
��Ͷ�����Һ�ȣ��ɽ������ν�һ������Ϊ����������ƽ���л�ѧ����ʽ�����������ת�Ʒ������Ŀ��
��![]() ��
��![]() ��
��![]() ��
��![]() ��
��![]() ��
��![]() ��
��![]() ______
______
��������������ˮ40L��ʹKCN��ȫת��Ϊ�����ʣ�������Һ��______g��
���𰸡�![]() ����
���� ![]() 80% c KCN�е�CԪ��
80% c KCN�е�CԪ�� 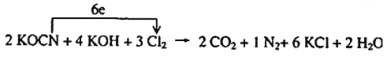 71
71
��������
(1)K=![]() ���¶����ߣ�K��С��˵���¶����ߣ�ƽ�������ƶ����淴ӦΪ���ȷ�Ӧ������ӦΪ���ȷ�Ӧ���ʴ�Ϊ��
���¶����ߣ�K��С��˵���¶����ߣ�ƽ�������ƶ����淴ӦΪ���ȷ�Ӧ������ӦΪ���ȷ�Ӧ���ʴ�Ϊ��![]() �����ȣ�
�����ȣ�
(2)��ƽ��ʱCO2��Ũ��Ϊx����CO��Ũ�ȼ�Сx��Ϊ![]() mol/L-x=0.1mol/L-x����K=4.0=
mol/L-x=0.1mol/L-x����K=4.0=![]() ����ã�x=0.08mol/L����
����ã�x=0.08mol/L����![]()
![]() =
=![]() ��CO��ƽ��ת����=
��CO��ƽ��ת����=![]() =80%��
=80%��
(3)a�����ٹ��������ƽ�ⲻ�ƶ���CO��ת���ʲ��䣬a����
b�����ӹ��������ƽ�ⲻ�ƶ���CO��ת���ʲ��䣬b����
c���Ƴ�����CO2��CO2��Ũ�ȼ�С��ƽ�������ƶ���CO��ת��������c��ȷ��
d����߷�Ӧ�¶ȣ�ƽ�ⳣ����С��CO��ת���ʼ�С��d����
e����С�ݻ�����ƽ�ⲻ�ƶ���CO��ת���ʲ��䣬e����
f��������������̵���ƽ���ʱ�䣬���Dz���ʹƽ�ⷢ���ƶ���CO��ת���ʲ��䣬f����
�ʴ�Ϊ��c��
(4)��KCN�е�CΪ+2�ۣ�KOCN�е�CΪ+4�ۣ�����KCN�е�CԪ�ر��������ʴ�Ϊ��KCN�е�CԪ�أ�
��1molCl2���뷴Ӧ��2mol���ӣ�KOCN����1molN2ʧ6mol���ӣ����ݵ�ʧ�����غ㣬����������ƽ��2![]() ~3Cl2~1N2~6KCl���ٸ���ԭ���غ�������ƽ����ԭ�ӣ����£�
~3Cl2~1N2~6KCl���ٸ���ԭ���غ�������ƽ����ԭ�ӣ����£�![]() �������ű�ʾ����ת�����£�
�������ű�ʾ����ת�����£�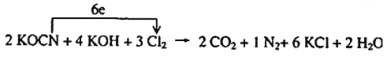 ���ʴ�Ϊ��
���ʴ�Ϊ��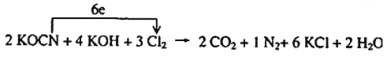 ��
��
�۸÷�����CN-������ΪN2�������¹�ϵ��2KCN~2![]() ~(2+3)Cl2��KCN������m=650mg/L��40L=26000mg=26g��
~(2+3)Cl2��KCN������m=650mg/L��40L=26000mg=26g��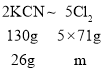 ����ã�m=71g���ʴ�Ϊ��71��
����ã�m=71g���ʴ�Ϊ��71��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ�Ͽɲ���CH3OH![]() CO+2H2�ķ�������ȡ�ߴ��ȵ�CO��H2���ҹ�������Աͨ�������ģ�⣬�о������ٻ���������״�����ķ�Ӧ������ͼ��ʾ�������������ٴ��������ϵ������ñ�ע������˵����ȷ���ǣ� ��
CO+2H2�ķ�������ȡ�ߴ��ȵ�CO��H2���ҹ�������Աͨ�������ģ�⣬�о������ٻ���������״�����ķ�Ӧ������ͼ��ʾ�������������ٴ��������ϵ������ñ�ע������˵����ȷ���ǣ� ��
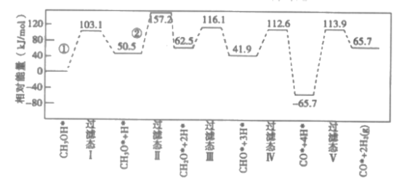
��֪���״�(CH3OH)���ⷴӦ�ĵ�һ�����̣������ֿ��ܷ�ʽ��
��ʽ��CH3OH*��CH3O*+H* Ea=+103.1 kJ��mol-1
��ʽ��CH3OH*��CH3*+OH* Eb=+249.3 kJ��mol-1
A.CH3OH*��CO*+2H2(g)����H>0
B.�٢ڶ�ΪO-H���Ķ��ѹ���
C.�ɻ��Eֵ�Ʋ⣬�״��ѽ������Ҫ�����ķ�ʽӦΪ��
D.�������εĻ�ѧ����ʽΪCHO*+3H*��CO*+4H*
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����0.2 L��NaCl��Һ��MgCl2��Һ��CuCl2��Һ��ɵĻ����Һ�У��������ӵ�Ũ����ͼ��ʾ��
(1)���Һ�У�NaCl�����ʵ���Ϊ_______mol��MgCl2������Ϊ_______g��
(2)�û����Һ��CuCl2�����ʵ���Ũ��Ϊ_____molL��1�����û����Һ��ˮϡ�������Ϊ1 L��ϡ�ͺ���Һ��Cu2+�����ʵ���Ũ��Ϊ_______molL��1��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����״���£�ij��̬������ϩ��(��һ��˫��)�Ļ������2.24 L��ȫȼ�պ����������建��ͨ��Ũ���ᣬŨ��������4.05 g��ʣ������ͨ����ʯ�ң���ʯ������6.60 g������ȡ2.24 L��״���µĸû�����壬����ͨ���������ˮ�У���ˮ����1.05 g��
(1)ȷ����������������������_______��
(2)���������������������������_______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���¹���ѧ�ҿ�������Ϊ�����ӵĽṹ�У�̼̼���Ե���˫�������϶��ɻ�״��Ϊ�����ۿ����յĹ۵㣬ijѧ�����������ʵ�鷽����
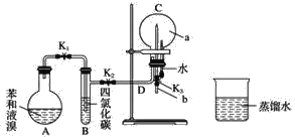
ʵ�������
�ٰ���ͼ��ʾ��װ��ͼ���Ӻø�������
�ڼ���װ�õ������ԣ�
����A�м��������ı���Һ��Ļ��Һ�壬�ټ����������ۣ�������Ƥ������K1��K2ֹˮ�У��ر�K3ֹˮ�У�
�ܴ���ƿC�������ռ���������b���¶˲����ձ����ˮ�У��ر�K2����K3����ѹԤ��װ��ˮ�Ľ�ͷ�ιܵĽ�ͷ���۲�ʵ������
��ش��������⣺
(1)��֤�������չ۵�����ʵ��������_________��
(2)A���������ķ�Ӧ�ķ�Ӧ����Ϊ__________��
(3)A�з�����Ӧ�Ļ�ѧ����ʽ__________��
(4)װ��B��������____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���״���Ϊȼ�ϣ��ڻ�ʯ��Դ�Ϳ�������Դʱ�ھ��й㷺��Ӧ��ǰ����
I. �״�����������ͺͲ�����Ϊ��ȼ��ȼ�ϡ�
��1�����͵���Ҫ�ɷ�֮һ������[C8H18(l)]����֪��25�桢101 kPaʱ��1 mol C8H18(l)��ȫȼ��������̬������̼��Һ̬ˮ���ų�5518 kJ�������÷�Ӧ���Ȼ�ѧ����ʽΪ______��
��2����֪��25�桢101 kPaʱ��CH3OH(l) + 3/2 O2(g) ==== CO2 (g) + 2H2O(l) �� H��-726.5 kJ/mol����ͬ�����ļ״�������ֱ���ȫȼ��ʱ���ų������϶����______��
��3��ij�о��߷ֱ��Լ״���������ȼ�ϣ�ʵ�����ڷ������߸��ɹ�������£�����β����CO�İٷֺ����������ļ������ܵĹ�ϵ������ʾ��
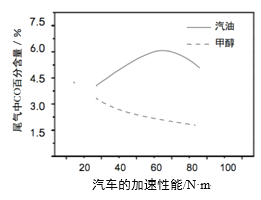
����ͼ��Ϣ��������������ȣ��״���Ϊȼ�ϵ��ŵ���______��
II. �״��ĺϳ�
��4����CO2(g)��H2(g)Ϊԭ�Ϻϳɼ״�����Ӧ�������仯����ͼ��ʾ��

�� ��ȫ��ͼ��ͼ��A��Ӧ����______��
�� �÷�Ӧ��Ҫ����ͭ��п����������������÷�Ӧ�Ħ�H______��������С�����䡱����
��5����֪�� CO(g)��1/2 O2(g) ==== CO2(g) ��H1��-283 kJ/mol
H2(g)��1/2 O2(g) ==== H2O(g) ��H2��-242 kJ/mol
CH3OH(g) + 3/2 O2(g) ==== CO2 (g) + 2H2O(g) ��H3��-676 kJ/mol
��CO(g)��H2(g)Ϊԭ�Ϻϳɼ״��ķ�ӦΪCO(g) + 2H2(g) ==== CH3OH(g) ���÷�Ӧ�Ħ�HΪ_____ kJ/mol��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����84������Һ����Ҫ�ɷ�Ϊ![]() ���㷺Ӧ����ɱ��������ij��ѧѧϰС���ü���ȼ�ϵ�ص�ⱥ��ʳ��ˮ�Ʊ���84������Һ��װ����ͼ��ʾ��
���㷺Ӧ����ɱ��������ij��ѧѧϰС���ü���ȼ�ϵ�ص�ⱥ��ʳ��ˮ�Ʊ���84������Һ��װ����ͼ��ʾ��![]() ��
��![]() ��
��![]() ��
��![]() ��Ϊ���Ե缫������˵����ȷ���ǣ� ��
��Ϊ���Ե缫������˵����ȷ���ǣ� ��
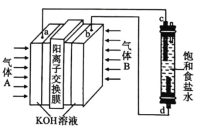
A.����B����
B.���װ���е��ܷ�ӦΪNaCl+H2O![]() NaClO+H2��
NaClO+H2��
C.����2.24L����״�������飬K+ͨ������Ĥ�������ƶ�0.8mol
D.���鷢���ĵ缫��Ӧ����ʽΪCH4-8e-+8OH��=CO2��+6H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�¶��£�40 g��10%��������Һ��60 g��7.5%����������Һ��ϣ��õ��ܶ�Ϊ1.20 g��cm-3�Ļ����Һ�����㣺
(1)�û����Һ�����ʵ���������Ϊ__��
(2)�û����Һ��NaNO3�����ʵ���Ũ��Ϊ__��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ�ϣ�������������ԭ��������β���е�CO��NO��
���������������������������Ϊ��Ӧ��2CO(g)��O2(g)![]() 2CO2(g)�Ĵ�����
2CO2(g)�Ĵ�����
ͼ�ױ�ʾ����ͬ�ĺ����ܱ���������ͬ��ʼŨ�ȡ���ͬ��Ӧʱ����£�ʹ��ͬ�����IJ�ͬ���������(���͡�����)��ʱ��CO��ת�������¶ȵĹ�ϵ��
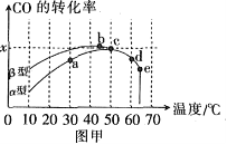
��1����a��b��c��d�ĵ��У�δ�ﵽƽ��״̬����___��
��2����֪c��ʱ������O2Ũ��Ϊ0.04mol��L-1����50��ʱ�������������������COת����Ӧ��ƽ�ⳣ��K=___(�ú�x�Ĵ���ʽ��ʾ)��
��3�����й���ͼ��˵����ȷ����__��
A.COת����Ӧ��ƽ�ⳣ��K(a)��K(c)
B.�ھ�δ�ﵽƽ��״̬ʱ��ͬ�������������������COת�����ʱ�����Ҫ��
C.b��ʱCO��O2����֮�䷢����Ч��ײ�ļ���������ʵ����������
D.e��ת���ʳ���ͻ���ԭ��������¶����ߺ����ʧȥ����
����ԭ��������ij���ܴ������Դ��������ͳ�β���е�̼��(C)��NOx����ͬ�¶��£���ģ��β��(��0.025molNO��0.5molO2������̼��)����ͬ������ͨ���ô�����������в���(CO2��N2��N2O)��NO��������ݣ������ͼ����ʾ��
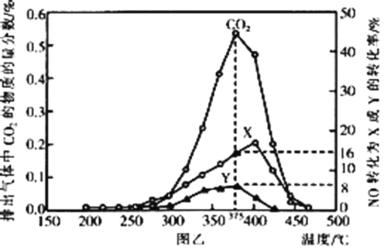
��4��375��ʱ������ų��������к�0.45molO2��0.052molCO2����Y�Ļ�ѧʽΪ___��
��5��ʵ������в���NOģ��NOx����������NO2��ԭ����___��
��6����ҵ�ϳ��ø�Ũ�ȵ�K2CO3��Һ����CO2�������õ�ⷨʹK2CO3��Һ��������װ��ʾ��ͼ��ͼ��
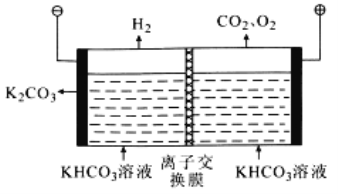
���������������ķ�Ӧ����___��H++HCO3�� =CO2��+H2O
�ڼ���CO32����������������ԭ����___��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com