
| 实验编号 | 反应物投入量 | 平衡时H2浓度 | 吸收或放出的热量 | 反应物转化率 |
| A | 1、1、0、0 | c1 | Q1 | α1 |
| B | 0、0、2、2 | c2 | Q2 | α2 |
| C | 2、2、0、0 | c3 | Q3 | α3 |
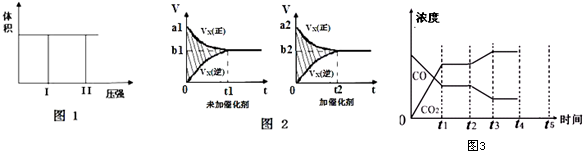
分析 Ⅰ.(1)正反应为气体物质的量减小的反应,容器的容积不变,由图可知,状态Ⅱ的压强大于状态Ⅰ压强的2倍,反应在绝热条件下进行,说明正反应为放热反应;正反应后气体的物质的量减少,所以混乱度减小,△H-T△S<0反应自发进行;
(2)加入催化剂,反应速率加快,到达平衡的时间缩短,平衡不移动,阴影部分为反应物浓度变化量,则两图中阴影部分面积相等;
(3)A.A、C两点都在等温线上,压强越大,反应速率越快;
B.A、C两点都在等温线上,反应前后气体物质的量不变,压强越大,容器的容积越小,而混合气体总质量不变;
C.B、C两点X的体积分数相同,则相同组分的体积分数相同;
D.压强相同,升高温度,化学平衡向吸热反应移动;
Ⅱ.(4)各物质起始物质的量均为1:1等于化学计量数之比,结合方程式可知,故平衡时n(CO)=n(H2O)、n(CO2)=n(H2),由于500℃时平衡常数K=$\frac{c({H}_{2})×c(C{O}_{2})}{c(CO)×c({H}_{2}O)}$=9可知,平衡时n(CO2)≠n(CO),则转化率不是50%;
B中转化到左边可以得到2molCO、2molH2O,恒温恒容下B、C是完全等效平衡,平衡时相同物质的浓度相同、物质的量相同;
恒温恒容下,C等效为在A的基础上增大压强,反应前后气体体积不变,平衡不移动,反应物转化率相等、相同物质的含量相等;
(5)在t2时刻后CO的浓度减小、CO2浓度增大,平衡向正反应方向移动,可以通过改变温度、改变水蒸气或氢气的量实现;
t4时刻通过改变容积的方法将压强增大为原先的两倍,则体积变为原来的一半,瞬间浓度分别增大为原来的2倍,由于反应前后气体系数相等,平衡不移动.
解答 解:Ⅰ.(1)正反应为气体物质的量减小的反应,容器的容积不变,由图可知,状态Ⅱ的压强大于状态Ⅰ压强的2倍,反应在绝热条件下进行,说明正反应为放热反应,则△H<0;正反应后气体的物质的量减少,所以混乱度减小,则△S<0,△H-T△S<0反应自发进行,该反应在低温条件下能自发进行,
故答案为:<;<;低温;
(2)加入催化剂,反应速率加快,所以b1<b2,到达平衡的时间缩短,所以t1>t2,平衡不移动,阴影部分为反应物浓度变化量,则两图中阴影部分面积相等,
故答案为:②③⑤;
(3)A. A、C两点都在等温线上,压强A点小于C点,压强越大速率越快,所以反应速率A<C,故A错误;
B. A、C两点都在等温线上,反应前后气体物质的量不变,压强越大,容器的容积越小,而混合气体总质量不变,所以气体密度:A<C,故B正确;
C. B、C两点X的体积分数相同,则相同组分的体积分数相同,所以气体的平均相对分子质量相同,故C错误;
D. 由状态B到状态A,压强相同,温度不同,正反应为放热反应,升高温度化学平衡向吸热反应移动,X的体积分数增大,所以可以通过升温使状态B到状态A,故D正确;
故答案为:BD;
Ⅱ.(4)各物质起始物质的量均为1:1等于化学计量数之比,结合方程式可知,故平衡时n(CO)=n(H2O)、n(CO2)=n(H2),由于500℃时平衡常数K=$\frac{c({H}_{2})×c(C{O}_{2})}{c(CO)×c({H}_{2}O)}$=9可知,平衡时n(CO2)≠n(CO),则转化率不是50%;
B中转化到左边可以得到2molCO、2molH2O,恒温恒容下B、C是完全等效平衡,平衡时相同物质的浓度相同、物质的量相同,则:c2=c3,B、C平衡时n(CO2)≠n(CO),转化率不是50%,故Q2≠Q3,设平衡时CO为ymol,则α3=$\frac{y}{2}$,α2=$\frac{2-y}{2}$,故α3+α2=1,可推知α3≠α2;
恒温恒容下,C等效为在A的基础上增大压强,反应前后气体体积不变,平衡不移动,反应物转化率相等、相同物质的含量相等,则:α1=α3,c3=2c1,Q3=2Q1,
结合上述分析可知:2c1=c2=c3 ,Q3=2Q1≠Q2=Q3 ,α1=α3≠α2 ,α1+α2=1,
故选:AD;
(5)在t2时刻CO的浓度减小、CO2浓度增大,平衡向正反应方向移动,且CO和CO2浓度变化有接触点,所以可以通过改变升高温度、增大水蒸气的量或减少氢气的量实现;
t4时刻通过改变容积的方法将压强增大为原先的两倍,则体积变为原来的一半,瞬间浓度分别增大为原来的2倍,由于反应前后气体系数相等,平衡不移动,在图中t4和t5区间内画出CO、CO2浓度变化曲线如图: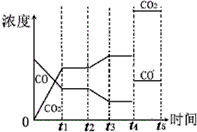 ,
,
故答案为:升高温度,或增加水蒸汽的量,或减少氢气的量; .
.
点评 本题考查化学平衡计算、化学平衡移动原理、平衡状态判断、化学平衡图象等,是对学生综合能力的考查,需要学生具备扎实的基础.


 长江作业本同步练习册系列答案
长江作业本同步练习册系列答案 小天才课时作业系列答案
小天才课时作业系列答案 一课四练系列答案
一课四练系列答案科目:高中化学 来源: 题型:选择题
| A. | 汽车尾气中的CO﹑NO等都是汽油和柴油的不完全燃烧产物 | |
| B. | 氢键﹑离子键﹑共价键都是微粒间的作用力,其中离子键和共价键属于化学键 | |
| C. | 高压钠灯发出的黄光射程远,透雾能力强,常用于道路和广场的照明 | |
| D. | 锅炉水垢中的硫酸钙可用碳酸钠饱和溶液处理,使之转化为碳酸钙,再用酸除去 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 利用二氧化碳制造全降解塑料,可以缓解温室效应 | |
| B. | 用电化学方法可在常温常压条件下合成氨,也可以用电解法精炼铜 | |
| C. | 检测NaClO、KMnO4等具有强氧化性物质溶液的PH时,最好选用PH计 | |
| D. | 纤维素经水解、发酵后可制得乙醇和少量甲醇,所得乙醇和甲醇的热值相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 熟石灰与水混合成糊状后会很快凝固,转化为坚硬的生石膏,可用它制作石膏绷带 | |
| B. | 人造纤维是利用自然界的非纤维材料通过化学合成方法得到的 | |
| C. | 雾霾是一种分散系,分散剂是空气,带活性炭口罩防雾霾的原理是吸附原理 | |
| D. | 利用二氧化碳等原料合成的聚碳酸酯类可降解塑料替代聚乙烯塑料,可减少“白色污染” |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 原子序数不可能为Z>Y>X | B. | X可能是非金属元素 | ||
| C. | Z一定在Y的下一周期 | D. | Y不可能在Z的下一周期 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
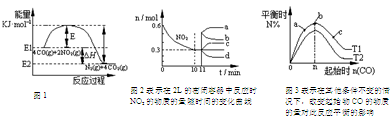
| A. | 在一定温度、固定容积的密闭容器里,混合气体的密度不再改变可以说明上述可逆反应已达平衡 | |
| B. | 由图1可得加入适当的催化剂,E减小,△H 增大 | |
| C. | 图3中T1和T2表示温度,对应温度下的平衡常数为K1、K2,则:T1<T2,K1<K2 | |
| D. | 图2中0~10min内该反应的平均速率v(CO)=0.03mol•L-1•min-1,从11min起其它条件不变,压缩容器的体积为1L,则n(NO2)的变化曲线为d |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
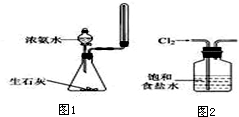
| A. | 用苯萃取溴水中的溴时,将溴的苯溶液从分液漏斗下口放出 | |
| B. | 用量筒量取20 mL 0.5000 mol•L-1H2SO4溶液于烧杯中,加水80mL配制成0.1000mol•L-1H2SO4溶液 | |
| C. | 实验室用图1所示装置制取少量氨气 | |
| D. | 实验室用图2所示装置除去Cl2中的少量HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将人群向高处疏散 | |
| B. | 将人群向顺风方向疏散 | |
| C. | 用浸有水或肥皂水(弱碱性)的毛巾捂住口鼻 | |
| D. | 向泄漏地点撒一些石灰 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 60mL 1mol•L-1氯化钠溶液 | B. | 75mL 1mol•L-1氯化钙溶液 | ||
| C. | 60mL 3mol•L-1氯化钾溶液 | D. | 75mL 1.5mol•L-1氯化铁溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com