
| (x+y)×14 |
| (x+2y)×16 |
| 7 |
| 12 |


科目:高中化学 来源: 题型:
| A、将固体加入容量瓶中溶解并稀释至刻度,配制成一定物质的量浓度的溶液 |
| B、用玻璃棒蘸取溶液,点在湿润的pH试纸上测定其pH |
| C、洗净的锥形瓶和滴定管可以放进烘箱中烘干 |
| D、氢氟酸试剂和NaOH溶液不可用带玻璃塞的玻璃瓶存放 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、金华米酒香甜可口,不含任何化学物质 |
| B、康师傅牌矿泉水,真正的纯水 |
| C、春晖牌蔬菜,天然种植,不含任何元素,真正的绿色食品 |
| D、云梦食用合格碘盐,可预防甲状腺肿大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、
| ||||||||||||||
B、春蚕到死丝方尽,
| ||||||||||||||
C、宝剑
| ||||||||||||||
D、莫道雪融便无迹,
|
查看答案和解析>>
科目:高中化学 来源: 题型:
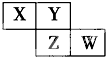 X、Y、Z、W均为短周期元素,它们在周期表中的位置如图所示.若Y原子的最外层电子数是内层电子数的3倍,下列说法中正确的是( )
X、Y、Z、W均为短周期元素,它们在周期表中的位置如图所示.若Y原子的最外层电子数是内层电子数的3倍,下列说法中正确的是( )| A、原子半径:W>Z>Y>X |
| B、最高价氧化物对应水化物的酸性:Z>W>X |
| C、与H2化合,Z比W更容易 |
| D、形成的气态氢化物溶于水,溶液呈碱性的是:X |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
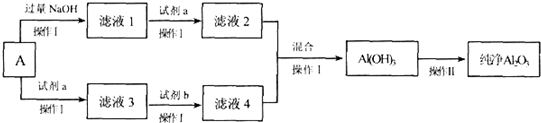
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com