
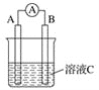
����Ŀ����1����ͼ��ʾ����CΪŨ���ᣬ������ָ�뷢��ƫת��B�缫����ΪFe ,A�缫����ΪCu����B�缫�ĵ缫��ӦʽΪ___________��A�缫�ĵ缫��ӦʽΪ_______����Ӧ����һ��ʱ�����ҺC��pH��___ (����ߡ������͡��������䡱)��
��2���ҹ��״�����������ˮ�����Ϊ��Դ�����͵ĺ�ˮ��־�ƣ��Ժ�ˮΪ�������Һ���������е�����ʹ����������������������ֻҪ�ѵƷ��뺣ˮ�����ӣ��ͻᷢ��ҫ�۵İ⡣���Դ�ĸ���������____��������ӦΪ___________��������ӦΪ_____________________________��
��3�����ε�ؾ��иߵķ���Ч�ʣ�����ܵ����ӣ�����Li2CO3��Na2CO3�������λ����������ʣ�COΪ����ȼ����������CO2�Ļ����Ϊ������ȼ�����Ƶ���650 ���¹�����ȼ�ϵ�أ�����йص�ط�Ӧʽ��������ӦʽΪ2CO��2CO32-��4e��=4CO2��������ӦʽΪ___________������ܷ�ӦʽΪ_______��
���𰸡�4H++ 2NO3��+2e-=2NO2��+2H2O Cu-2e-=Cu2+ ���� �� 4Al��12e��=4Al3�� 3O2��6H2O��12e��=12OH�� O2��2CO2��4e��=2CO 2CO��O2=2CO2
��������
��1������ͭ��������Ũ�������������Һ����������Ũ�����лᷢ���ۻ�������ͭ�Ǹ����������������ڸ�����ͭʧȥ���ӱ��ͭ���ӣ�����������Һ�е���������ӵõ������ɶ�������������������Ӧ���������ӣ�������Һ��pH���ߣ��ʴ�Ϊ��4H++2NO3��+2e-=2NO2��+2H2O�� Cu-2e-=Cu2+�����ߣ�
��2����-����-��ˮ����У����������е����������������������������������������ڸ�������ʧȥ���ӱ�������ӣ���������������õ��ӡ��ʴ�Ϊ������4Al��12e��=4Al3����3O2��6H2O��12e��=12OH����
��3��һ����̼�Ǹ���ȼ���������Ͷ�����̼�Ļ������������ȼ������ص��ܷ�Ӧ����һ����̼ȼ�յķ�Ӧ����2CO+O2=2CO2�����ܷ�Ӧʽ��ȥ������Ӧʽ�����ɵ�������Ӧʽ���ʴ�Ϊ��O2��2CO2��4e��=2CO�� 2CO��O2=2CO2��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2018�꣬�����˳��ˡ�����Э����ʵ���ٹ�ҵ��ս�ԣ����й�ȴ�Ӵ��˻������ȣ�����ڹ�����ҹ������εĴ���������ҹ�������ǿ��������CO2���⻯�ϳɼ״������Ĺ�ҵ�������о���ʵ�ֿɳ�����չ��
��1����֪��CO2(g)+H2(g)![]() H2O(g) +CO(g)����H1 = + 41.1 kJmol-1
H2O(g) +CO(g)����H1 = + 41.1 kJmol-1
CO(g)+2H2(g)![]() CH3OH(g)����H2=��90.0 kJmol-1
CH3OH(g)����H2=��90.0 kJmol-1
д��CO2���⻯�ϳɼ״����Ȼ�ѧ����ʽ��_______��
��2��Ϊ���CH3OH���ʣ�������Ӧ���õ�������_______������ĸ����
a.���¸�ѹ b.���µ�ѹ c.���µ�ѹ d.���¸�ѹ
��3��250�桢�ں����ܱ���������CO2(g)���⻯�ϳ�CH3OH(g)����ͼΪ��ͬͶ�ϱ�[n(H2)/n(CO2)]ʱij��Ӧ��Xƽ��ת���ʱ仯���ߡ�
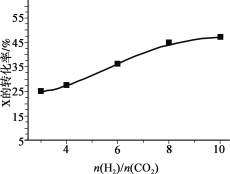
�� ��Ӧ��X��_______������CO2������H2������
�� �������_______��
��4��250�桢�����Ϊ2.0L�ĺ����ܱ������м���6mol H2��2mol CO2�ʹ�����10minʱ��Ӧ�ﵽƽ�⣬���c(CH3OH) = 0.75 mol�� L��1��
�� ǰ10min��ƽ����Ӧ����v(H2)��_______ mol��L��1��min ��1��
�� ��ѧƽ�ⳣ��K = _______��
�� �����ͷ�Ӧ�����뷴Ӧ��ת���ʺͲ����ѡ�����и߶���ء�������ͬͶ�ϱȺ���ͬ��Ӧʱ�䣬����ʵ���������£�
ʵ���� | �¶ȣ�K�� | ���� | CO2ת���ʣ�%�� | �״�ѡ���ԣ�%�� |
A | 543 | Cu/ZnO���װ� | 12.3 | 42.3 |
B | 543 | Cu/ZnO����Ƭ | 11.9 | 72.7 |
C | 553 | Cu/ZnO���װ� | 15.3 | 39.1 |
D | span>553 | Cu/ZnO����Ƭ | 12.0 | 70.6 |
�����ϱ��������ݣ���CO2�����״�������ѡ��Ϊ_______������ĸ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ӷ���ʽ��д��ȷ����
A.��CH3COOH�м�������NaOH��Һ��H��+OH��=H2O
B.Fe��ϡHNO3��Ӧ��Fe+2H��=Fe2��+H2��
C.Cl2ͨ��H2O�У�Cl2+H2O=2H++Cl��+ClO��
D.AlCl3��Һ�м��������ˮ��Al3++3NH3��H2O=Al(OH)3��+3![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и�ѡ���У������������α�ʾΪX��Y��Z��������ͼ������Բ��ʾ�Ĵ�����ϵ��������ǣ�

A. ����������������
B. ������������������������
C. ���塢��ɢϵ�������
D. ���ֽⷴӦ���û���Ӧ����ѧ��Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��E�dz��л�ѧ���������ʣ����ᡢ�������ơ��������ơ�̼���ơ�������̼�е�ijһ�֡�A�����ڽ���������⣬B�������������������������֮�䷢����Ӧ��ת���Ĺ�ϵ����ͼ��ʾ����������ʾ�������ʼ��ܷ�����Ӧ����������ʾ�������ʼ��ת����ϵ����

��1��A��C�Ļ�ѧʽ�ֱ�Ϊ________��________��D������������е�һ����;��_________��
��2��E��D��Ӧ�Ļ�ѧ����ʽΪ_____________________________��B��D��Ӧ�Ļ�ѧ����ʽΪ_________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ������Ҫ0.1mol��L��1 NaOH��Һ450 mL��������Һ����������ش��������⡣
(1)����ͼ��ʾ�����У�����������Һ�϶�����Ҫ���� _____________(�����)����ͼ�����������⣬����������Һ����Ҫ�IJ������� _____________________��
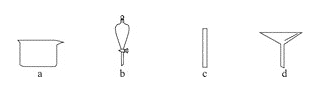
(2)����ʱ������ȷ�IJ���˳����(����ĸ��ʾ��ÿ������ֻ��һ��) __________��
A��������ˮϴ���ձ�2�Ρ�3�Σ�ϴ��Һ��ע������ƿ����
B����ʢ��NaOH������ձ��м�������ˮ�ܽ�
C�����ձ�������ȴ����Һ�ز�����ע������ƿ��
D��������ƿ�ǽ����������µߵ���ҡ��
E�����ý�ͷ�ιܼ�ˮ��ʹ��Һ��Һ��ǡ����̶�����
F������������ƿ��С�ļ�ˮ��ֱ��Һ��ӽ��̶�1 cm��2 cm��
(3)ʵ�������õ��������������÷ֱ��ǣ������� ______�������� ________��
(4)��������ƿ��������������������ȷŨ����Һ��������������������Һ���������������ȣ���ʹ��֮ǰҪ����Ƿ�©ˮ����Щ��������ȷ���� ________��
A���٢ڢۢ�������B���ڢ� C���٢ڢ� D���ڢۢ�
(5)���ݼ�����������ƽ��ȡ������Ϊ ____________g��
(6)���в������Ƶ���ҺŨ��ƫ�͵���______��
A������NaOHʱ����NaOH����ֽ�ϳ���
B������ǰ������ƿ������������ˮ
C������ʱ��NaOHδ��ȴֱ�Ӷ���
D��������ƿ��ת����Һʱ������Һ����������ƿ����
E������ʱ���ӿ̶���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪����ԭ��HSO3-��I����������IO3-��I2���ں�3 mol NaHSO3����Һ����μ���KIO3��Һ������KIO3������I2�����ʵ����Ĺ�ϵ������ͼ��ʾ��
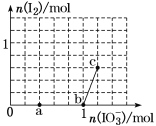
����˵����ȷ����(����)
A.0��b��ķ�Ӧ�������ӷ���ʽ3SO32-��IO3-=3SO42-��I����ʾ
B.a��ʱ���ĵ�NaHSO3�����ʵ���Ϊ1.2 mol
C.b�㵽c�㣬KIO3��NaHSO3��Ӧ����I2
D.����Һ��I����I2�����ʵ���֮��Ϊ5��3ʱ�������KIO3Ϊ1.08 mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ԭ��Ӧ��һ����Ҫ�ķ�Ӧ���ڹ�ũҵ�������ճ������ж��й㷺����;���ش������й�������ԭ�����⡣
��.������ԭ��Ӧ��ʵ���ϰ��������ͻ�ԭ�������̡�������һ����ԭ���̵ķ�Ӧʽ��NO3-+4H++3e-��NO+2H2O��KMnO4��Na2CO3��Cu2O��Fe2(SO4)3���������е�һ�����ʣ��ף���ʹ������ԭ���̷�����
��1�����ʣ��ף�Ϊ_________�����ѧʽ��
��2����Ӧ�������������4.48LNO���壬��ת�Ƶ��ӵ���Ŀ�� ____________��
��.�������ƣ�NaNO2����ʳ��һ������ζ�����к�ǿ�Ķ��ԣ���ʳNaNO2��ʹ���ж�����֪���������ܷ������·�Ӧ��2NaNO2 + 4HI �T 2NO�� + 2NaI + I2 + 2H2O
��1����˫���ű���÷�Ӧ�ĵ���ת�Ʒ�����Ŀ��_______���������뻹ԭ�������ʵ���֮��Ϊ______��
��2���ⶨNaNO2�����������Ĺ������£���ȡNaNO2��Ʒ0.6 g����ƿ�У��ȼ�ˮ�ܽ⣬�������еμ�0.1 mol��L��1����KMnO4��Һ��ǡ����ȫ��Ӧʱ����������KMnO4��Һ24mL������װ��C�����ù�����NaNO2����������___________������֪�ⶨ�����з�����Ӧ�ķ���ʽΪMnO4����NO2����H����Mn2+��NO3����H2O��δ��ƽ���������ʲ���KMnO4��Ӧ��
��3������ˮ�е�NO3�������ཡ������Σ����Ϊ�˽�������ˮ��NO3����Ũ�ȣ�ij�о���Ա������ַ�����
�ٷ���a��������������Fe��OH��2��ԭNO3��������ΪNH3������3.4g NH3ͬʱ������_____molFe(OH)3��
�ڷ���b��������������Al�ۻ�ԭNO3����������N2�������ķ�Ӧ�ɱ�ʾ���£���ɷ���ʽ����ƽ��
____Al��____NO3����____ ��____����____AlO2����______N2����____��____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijҺ̬±����RX��R�������X��ij��±��ԭ�ӣ����ܶ���ag/cm3 ����RX���Ը�ϡ���ˮ�ⷴӦ����ROH���ܸ�ˮ���ܣ���HX��Ϊ�˲ⶨRX����Է����������ⶨ��ʵ�鲽�����£�
��ȷ��ȡ��±���� b mL��������ƿ�С�������ƿ�м������ϡNaOH��Һ�����ϴ��г������ܵ����ӣ����ȣ�������Ӧ���۷�Ӧ��ɺ���ȴ��Һ����ϡHNO3�ữ���μӹ���AgNO3��Һ���ð�ɫ�������ܹ��ˣ�ϴ�ӣ��������أ��õ�cg���塣�ش��������⣺
��1��װ���г������ܵ�������________________________��
��2��������У�ϴ�ӵ�Ŀ����Ϊ�˳�ȥ������������__________________���ӡ�
��3����±����������±�ص�������_____���жϵ�������______________��
��4����±�������Է���������____________________�����ú�a��b��c�Ĵ���ʽ��ʾ��
��5������ڲ�����м�HNO3�������㣬û�н���Һ�ữ��������в�õ�cֵ��������ѡ����룩___________��
A��ƫ��B��ƫС����C����С��������D������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com