
有以下四种物质:① 标况下11.2L CO2 ②1g H2 ③1.204×1024个N2 ④4℃时18 mLH2O,下列说法不正确的是:
A.分子个数:③>④>①=② B.体 积:③>④>①=②
C.原子个数:③>④>①>② D.质 量:③>①>④>②
 同步练习河南大学出版社系列答案
同步练习河南大学出版社系列答案科目:高中化学 来源: 题型:
下列叙述正确的是( )
|
| A. | 1mol H2O的质量为18g/mol |
|
| B. | CH4的摩尔质量为16g |
|
| C. | 3.01×1023个SO2分子的质量为32g |
|
| D. | 标准状况下,1mol任何物质体积均为22.4L |
查看答案和解析>>
科目:高中化学 来源: 题型:
高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂。其生产工艺如下:
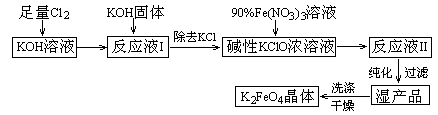 |

已知:① 2KOH + Cl2 → KCl + KClO + H2O(条件:温度较低)
② 6KOH + 3Cl2 →5KCl + KClO3 + 3H2O(条件:温度较高)
③ 2Fe(NO3)3 +3KClO+10KOH →2K2FeO4 + 6KNO3 + 3KCl + 5H2O
回答下列问题:
(1)该生产工艺应在温度 (填“较高”或“较低”)的情况下进行;
(2)写出工业上制取Cl2的化学方程式 ;
(3)K2FeO4具有强氧化性的原因 ;
(4)配制KOH溶液时,是在每100 mL水中溶解61.6 g KOH固体(该溶液的密度为1.47 g/mL),它的物质的量浓度约为 。
(5)在“反应液I”中加KOH固体的目的是 (选填序号)。
A.与“反应液I”中过量的Cl2继续反应,生成更多的KClO
B.KOH固体溶解时会放出较多的热量,有利于提高反应速率
C.为下一步反应提供反应物
D.使副产物KClO3转化为 KClO
(6)从“反应液II”中分离出K2FeO4后,会有副产品 (写化学式),它们都是重要的化工产品,具体说出其中一种物质的用途 。
查看答案和解析>>
科目:高中化学 来源: 题型:
请写出下列化学反应方程式:
(1)乙烯通入溴水中: ▲
(2)2-氯丙烷与氢氧化钠水溶液共热: ▲
(3)乙醇和乙酸在浓硫酸作用下反应: ▲
(4)苯酚与甲醛在加入浓盐酸作用下发生缩聚反应: ▲
查看答案和解析>>
科目:高中化学 来源: 题型:
下列物质在水溶液中的电离方程式书写正确的是( )
A.KClO3=K++3O2—+Cl5+ B.NaHSO4 = Na++HSO4—
C.H2SO4=H++ SO42— D.Al2(SO4)3 = 2Al3++3SO42—
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中正确的是( )
A.加入碳酸钠溶液产生白色沉淀,再加盐酸,白色沉淀消失,一定有Ca2+
B.用玻璃棒蘸取新制氯水,点在PH试纸的中央,与标准比色卡比较,测定氯水的PH
C.某溶液与NaOH溶液共热,产生使湿润红色石蕊试纸变蓝气体,说明原溶液中存在NH4+
D.加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42—
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com