
| ���� | ����ƽ�ⳣ����Ka��Kb�� |
| CH3COOH | 1.8��10-3 |
| HNO3 | 4.6��10-4 |
| HCN | 5��10-10 |
| HClO | 3��10-8 |
| NH3?H2O | 1.8��10-5 |
| 0.0001mol/L��0.5L |
| 0.01mol/L |


 ��ǰ����ϵ�д�
��ǰ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
 �ס�����λͬѧ�����ʵ��ȷ��ij��HA��������ʣ����ڵ���ƽ�⣬�Ҹı�����ƽ�ⷢ���ƶ���ʵ�鷽�����£�
�ס�����λͬѧ�����ʵ��ȷ��ij��HA��������ʣ����ڵ���ƽ�⣬�Ҹı�����ƽ�ⷢ���ƶ���ʵ�鷽�����£�| 1 | 25 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
��8�֣��ס�����λͬѧ�����ʵ��ȷ��ij��HA��������ʣ����ڵ���ƽ�⣬�Ҹı�����ƽ�ⷢ���ƶ���ʵ�鷽�����£�
�ף���ȷ����0.1mol��L-1��HA��HCl��Һ��100mL��
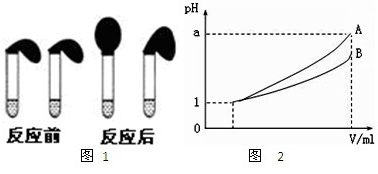
��ȡ������ͬ����������С��ȵ�п��������ֻ�Թ��У�ͬʱ����0.1mol��L-1��HA��HCl��Һ��100mL������ͼװ�ã��۲�����
�ң�����pH�Ʋⶨ���ʵ���Ũ�Ⱦ�Ϊ0.1mol��L-1��HA��HCl��Һ��pH��
����ȡ0.1mol��L-1��HA��HCl��Һ��2�Σ�1��ԼΪ![]() ���ֱ�ϡ����100mL��
���ֱ�ϡ����100mL��
����pH�Ʋ���pH�仯��
��1���ҷ�����˵��HA��������ʵ������ǣ����0.1mol��L-1��HA��Һ��pH 1���>����<����=�����������У�˵��HA��������ʵ�ʵ�������� ��
A��װHCl���Թ��зų����������ʴ�
B��װHA��Һ���Թ��зų����������ʴ�
C�������Թ��в�����������һ����
��2����ͬѧ��Ƶ�ʵ��ڢڲ�����֤���ı���������ƽ�ⷢ���ƶ�����ˮϡ�ͣ�����HA�ĵ���̶� �������С�����䡱��
��3����ͬѧΪ�˽�һ��֤��������ʵ���ƽ���ƶ���������������ʵ�飺ʹHA�ĵ���̶Ⱥ�c��H+������С��c��A��������0.1mol��L-1��HA��Һ�У�ѡ����� �Լ���
A��NaA���壨����ȫ����ˮ�� B��1mol��L-1NaOH��Һ
C��1mol��L-1H2SO4 D��2mol��L-1HA
��4��pH=1����������ҺA��B��1mL���ֱ��ˮϡ�͵�1000mL����pH����Һ���V�Ĺ�ϵ����ͼ��ʾ��������˵������ȷ����
A����a=4����A��ǿ�ᣬB������
B����![]() ����A��B��������
����A��B��������
C����������Һ�����ʵ�������һ�����
D��ϡ�ͺ�A��Һ�����Ա�B��Һ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ʡģ���� ���ͣ������

 CH3CH2OH(g)+3H2O(g) ��H��a kJ/mol ��һ��ѹǿ�£����������Ӧ��ʵ���������±���
CH3CH2OH(g)+3H2O(g) ��H��a kJ/mol ��һ��ѹǿ�£����������Ӧ��ʵ���������±��� 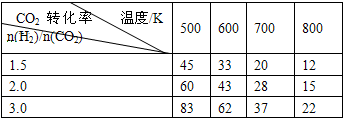

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ʡģ���� ���ͣ������

 CH3CH2OH(g)+3H2O(g) ��H��a kJ/mol ��һ��ѹǿ�£����������Ӧ��ʵ���������±���
CH3CH2OH(g)+3H2O(g) ��H��a kJ/mol ��һ��ѹǿ�£����������Ӧ��ʵ���������±��� 

�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com