
【题目】某同学做了如下实验:
装置 |
|
|
现象 | 电流计指针未发生偏转 | 电流计指针发生偏转 |
下列说法中不正确的是
A. 往铁片Ⅰ所在烧杯加入蒸馏水,电流表指针会发生偏转
B. 用K3[Fe(CN)3]溶液检验铁片Ⅲ、Ⅳ附近溶液,可判断电池的正、负极
C. 铁片Ⅰ、Ⅲ的腐蚀速率不相等
D. “电流计指针未发生偏转”,铁片Ⅰ、铁片Ⅱ均未被腐蚀
【答案】D
【解析】
A项,往铁片Ⅰ所在烧杯加入蒸馏水,造成两溶液中氯化钠的浓度不相等,存在电势差,有电流产生,电流表指针会发生偏转,故A项正确;
B项,图2中因两溶液中氯化钠的浓度不相等,因此发生的是电化学腐蚀,且浓度大的一极发生的反应是Fe-2e-=Fe2+,可以用K3[Fe(CN)3]溶液检验亚铁离子的存在,进而判断电池的正、负极,故B项正确;
C项,铁片Ⅰ、Ⅲ所处的电解质溶液浓度相同,但因为Ⅲ发生的是电化学腐蚀,Ⅰ是普通腐蚀,所以速率不同,故C项正确;
D项,图1中因两溶液中氯化钠的浓度相等,因此发生的是普通的化学腐蚀,且腐蚀速率相等,电流计指针未发生偏转,但铁片Ⅰ、铁片Ⅱ均被腐蚀,故D项错误;
综上所述,本题选D。


 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案 初中学业考试导与练系列答案
初中学业考试导与练系列答案科目:高中化学 来源: 题型:
【题目】下列溶液中溶质的物质的量浓度为1mol/L的是( )
A. 将58.5g NaCl溶解在1L水中
B. 将1L 10mol/L的硫酸加入9L水中
C. 将11.2L HCl气体溶于水配成0.5L溶液
D. 将40g NaOH溶解在少量水中,再加蒸馏水直到溶液体积为1L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学在研究新制饱和氯水成份的实验中,根据实验现象得出的结论不正确的是( )
A. 氯水的颜色呈浅黄绿色,说明氯水中含有Cl2
B. 向氯水中滴加硝酸酸化的AgNO3溶液,产生白色沉淀,说明氯水中含有CI-
C. 向氯水中加入NaHCO3粉末,有气泡产生,说明氯水中含有H+
D. 向淀粉碘化钾溶液中滴加少量氯水,溶液变蓝,说明氯水中含有ClO-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在标准状况下,m g气体A与n g气体B的分子数相同,下列说法中不正确的是
A. 两种气体A与B的相对分子质量之比为m∶n
B. 同质量气体A与B的分子数之比为n∶m
C. 同温同压下,A、B两气体的密度之比为n∶m
D. 相同状况下,同体积A、B两气体的质量之比为m∶n
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用电化学制备正十二烷的方法:向烧杯中加入50 mL 甲醇,不断搅拌加入少量金属钠,再加入11 mL正庚酸搅拌均匀,装好铂电极,接通电源反应,当电流明显减小时切断电源,然后提纯正十二烷。已知电解总反应: 2C6H13COONa+2CH3OH![]() C12H26+2CO2↑+H2↑+2CH3ONa,下列说法不正确的是
C12H26+2CO2↑+H2↑+2CH3ONa,下列说法不正确的是

A. 图中电源的a极为直流电源的负极
B. 电解过程中离子浓度会不断降低
C. 阳极电极反应:2C6H13COO--2e-=C12H26+2CO2↑
D. 反应一段时间后将电源正负极反接,会产生杂质影响正十二烷的制备
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁铬氧化还原液流电池是一种低成本的储能电池,电池结构如图所示,工作原理为Fe3++Cr2+![]() Fe2++Cr3+。下列说法正确的是
Fe2++Cr3+。下列说法正确的是

A. 电池充电时,b极的电极反应式为Cr3++e-=Cr2+
B. 电池充电时,Cl-从a极穿过选择性透过膜移向b极
C. 电池放电时,a极的电极反应式为Fe3++3e-=Fe
D. 电池放电时,电路中每通过0. 1 mol电子,Fe3+浓度降低0. 1 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在给定条件下,下列选项所示的物质间转化均能实现的是( )
A. SO2![]() CaSO3
CaSO3![]() CaSO4
CaSO4
B. Fe![]() Fe2O3
Fe2O3![]() FeCl3
FeCl3
C. HCl(aq) ![]() Cl2
Cl2![]() Ca(ClO)2
Ca(ClO)2
D. Cu2(OH)2CO3![]() CuO
CuO![]() CuCl2(aq)
CuCl2(aq)
查看答案和解析>>
科目:高中化学 来源: 题型:
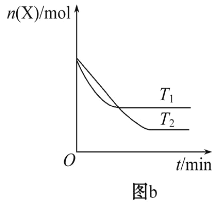
【题目】T0 ℃时,在2 L的密闭容器中发生反应:X(g)+Y(g)![]() Z(g)(未配平),各物质的物质的量随时间变化的关系如图a所示。其他条件相同,温度分别为T1 ℃、T2 ℃时发生反应,X的物质的量随时间变化的关系如图b所示。下列叙述正确的是
Z(g)(未配平),各物质的物质的量随时间变化的关系如图a所示。其他条件相同,温度分别为T1 ℃、T2 ℃时发生反应,X的物质的量随时间变化的关系如图b所示。下列叙述正确的是
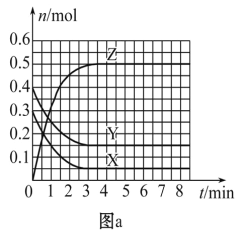
A. 该反应的正反应是吸热反应
B. T0 ℃,从反应开始到平衡时:v(X)=0. 083 mol·L-1·min-1
C. 图a中反应达到平衡时,Y的转化率为37. 5%
D. T1℃时,若该反应的平衡常数K=50,则T1<T0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上用重铬酸钠(Na2Cr2O7)结晶后的母液(含少量杂质Fe3+)生产重铬酸钾 (K2Cr2O7),其工艺流程及相关物质溶解度曲线如下图所示。


(1)向Na2Cr2O7母液中加碱液调pH的目的是_____________________。
(2)通过冷却结晶析出大量K2Cr2O7的原因是________________________________。
(3)固体A的主要成分为__________(填化学式),用热水洗涤固体A,回收的洗涤液转移到母液___________(填“I”“Ⅱ”或“Ⅲ”)中,既能提高产率又可使能耗降低。
(4)测定产品中K2Cr2O7含量的方法如下:称取产品试样2.500 g 配成250 mL溶液,用移液管取出25.00 mL于碘量瓶中,加入10 mL 2 mol·L-l H2SO4溶液和足量KI溶液(铬的还原产物为Cr3+),放置于暗处5 min,然后加入100 mL蒸馏水、3 mL 淀粉指示剂,用0.1200 mol·L-l Na2S2O3标准溶液滴定(已知I2+ 2S2O32-=2I-+S4O62-)。
①酸性溶液中KI 与K2Cr2O7反应的离子方程式为_____________________________。
②若实验中共用去Na2S2O3标准溶液40.00 mL,则所得产品中重铬酸钾的纯度为__________%( 保留2 位小数,设整个过程中其他杂质不参与反应)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com