
【题目】NA表示阿伏伽德罗常数,下列叙述正确的是( )
A.0.1 mol丙烯酸中含有双键的数目为0.1NA
B.标准状况下,11.2 L苯中含有分子的数目为0.5NA
C.1 mol甲苯含有6nA个C—H键
D.丙烯和环丙烷组成的42 g混合气体中氢原子的个数为6NA
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】下图所示的实验装置中, A、E分别为NH3和Cl2的发生装置。
请回答下列问题:
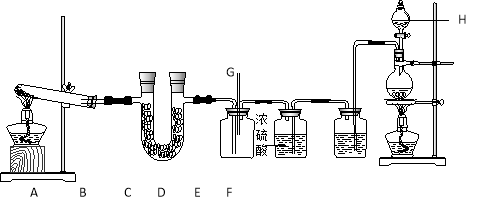
(1)装置E中发生反应的离子方程式为 。
(2)甲、乙两同学分别采用下列两种方案制取C12:甲:用含HCl 146g的浓盐酸与足量的MnO2反应。乙:用87g MnO2与足量浓盐酸反应。则所得氯气__________(填字母)。
a.甲比乙多 b.乙比甲多 c.一样多
(3)仪器H的名称是_____________(填名称) ,装置D的作用是 。
(4)装置C的导管G处逸出的尾气中可能含有黄绿色的有毒气体,可用 进行尾气处理(填选用试剂的名称)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下将足量的炭和2 mol水蒸气混合于1 L的密闭容器中,发生如下反应:C(s)+H2O(g) ![]() CO(g)+H2(g),
CO(g)+H2(g),
(1)该反应平衡常数K的表达式
(2)已知在700 ℃时,该反应的平衡常数K1=0.6,1000 ℃时,该反应的平衡常数K2为1.0,则该反应为的ΔH (填“<0”或“>0”)。
(3)能判断该反应达到化学平衡状态的依据是________。(填编号)
A、容器中气体的密度不变
B、生成a mol CO的同时消耗a mol H2
C、c(H2O)=c(CO)
D、混合气体的平均相对分子质量不变
(4)在1 000 ℃下,某时刻CO的物质的量为1.0 mol,则此时v正________v逆(填“>”、“=”或“<”),此时H2O(g)的转化率为________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用甲烷和氯气发生取代反应制取副产品盐酸的设想在工业上已成为现实。某化学兴趣小组通过在实验室中模拟上述过程,其设计的模拟装置如下图所示:
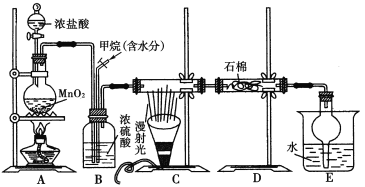
根据要求填空:
(1)B装置有三种功能:①控制气流速度;②干燥混合气体;③________________。
(2)设V(Cl2)/V(CH4)=x,若理论上欲获得最多的氯化氢,则x值应____________。
(3)在C装置中,经过一段时间的强光照射,发现硬质玻璃管内壁有黑色小颗粒产生,写出置换出黑色小颗粒的化学方程式:____________________________________。
(4)E装置除生成盐酸外,还含有有机物,从E中分离出盐酸的最佳方法为___________。该装置的主要缺陷是 。
(5)已知丁烷与氯气的取代反应的产物之一为C4H8Cl2,其有 种同分异构体。
查看答案和解析>>
科目:高中化学 来源: 题型:
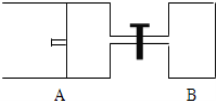
【题目】如图所示,向A中充入1mol X和1mol Y,向B中充入2mol X和2mol Y,起始时,V(A)=V(B)=a L.在相同温度和有催化剂存在的条件下,两容器中各自发生下述反应:X(g)+Y(g)2Z(g)+W(g)△H<0
达到平衡时,V(A)=1.2aL.试回答:
(1)A中X的转化率α(X)= 。
(2)A、B中X转化率的关系:α(A) α(B)(填“>”“=”或“<”)。
(3)平衡时的压强:P(B) 2P(A)(填“>”“=”或“<”)。
(4)打开K,一段时间又达平衡时,A的体积为 L(连通管中气体体积不计)。
(5)在(3)达平衡后,同时等幅升高A、B的温度,达新平衡后A的体积 (填“变大”“不变”或“变小”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水是巨大的资源宝库,从海水中提取食盐和溴的过程如下:
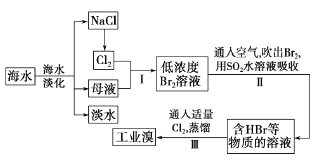
(1)请列举海水淡化的两种方法:________、_________。
(2)步骤I中己获得Br2,步骤II中又将Br2还原为Br-。其目的是_____。
(3)步骤II用SO2水溶液吸收Br2,吸收率可达95% 。有关反应的离子方程式为_________。
(4)某化学研究性学习小组为了了解从工业溴中提纯溴的方法。查阅了有关资料知:Br2的沸点为59 ℃.微溶于水,有毒并有强腐蚀性。他们参观生产过程后.画了如下装置简图:
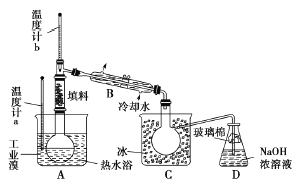
请你参与分析讨论:
①图中仪器B的名称是_______。
② 整套实验装皿中仪器连接均不能用橡胶塞和橡胶管。其原因是_______。
③ 实验装置气密性良好,要达到提纯溴的目的,操作中如何控制关键条件?_______。
④ C中液体颜色为_______。为除去该产物中仍残留的少量Cl2,可向其中加入NaBr,溶液,充分反应后.再进行的分离操作是_______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com