
| A.非金属性: P>S>Cl | B.碱性:NaOH>KOH>RbOH |
| C.气态氢化物稳定性:HF>HCl>HBr | D.酸性:H2SO4>HClO4>HBrO4 |
 提分百分百检测卷系列答案
提分百分百检测卷系列答案 宝贝计划期末冲刺夺100分系列答案
宝贝计划期末冲刺夺100分系列答案 能考试全能100分系列答案
能考试全能100分系列答案科目:高中化学 来源:不详 题型:单选题

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
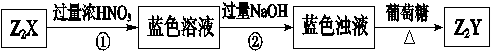
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
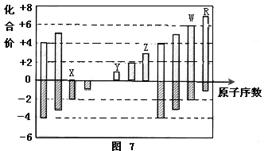
| A.原子半径:Z>Y>X |
| B.气态氢化物的稳定性:W>R |
| C.WX3和水反应形成的化合物是离子化合物 |
| D.Y和Z两者最高价氧化物对应的水化物能相互反应 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.甲烷的电子式:  |
B.氮原子的L层电子排布图: |
| C.硫离子的核外电子排布式:1s22s22p63s23p4 |
| D.碳12原子: 612C |
查看答案和解析>>
科目:高中化学 来源:不详 题型:推断题


查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com