
����Ŀ��(1)�����£�����Ũ��Ϊ0.1mol/L��FeSO4��Һ���о���ͬpH��Fe2+������Ӱ�죬�������ͼ��ʾ��(���跴Ӧ��������Һ�������)

��pH��5.5�Ļ����£��÷�Ӧ��0��15min��ƽ������v(Fe2+)��______��������ҺpH��Fe2+����������_______________(����������С������Ӱ�족)��
(2)��pH��13�Ļ����£�Fe2+���������ʿ�������Ϊ:��һ��:Fe2++2OH����Fe(OH)2���ڶ���__________________________(�û�ѧ����ʽ�ش�)�������ﵽƽ��ʱ��c( Fe2+) /c(Fe3+)__________4.0��1022(�>����<����=��)����֪Ksp[Fe(OH)3]��2.5��10��39�� Ksp[Fe(OH)2]��1.0��10��15
(3)��ҵ�Ͽ���H2��ԭ������NO����Ӧԭ��Ϊ:2NO(g)+2H2(g) ==N2(g)+2H2O(g): ��H��a��֪�ڱ�״������Ԫ�����ȶ��ĵ�������1mol��������ʱ���ʱ�б�Ħ�������ʡ�NO(g)��H2O(g)�ı�Ħ�������ʷֱ�Ϊ+90kJ/mol��-280 kJ/mol����a=_______��
(4)��֪2NO(g)+O2(g)![]() 2NO(g) ��H= ��110 kJ��mol��1;25��ʱ����NO��O2�����ʵ���֮��Ϊ2:1������Է�Ӧ�������ò�ѹ���о��䷴Ӧ�Ľ����������ϵ����ѹǿp��ʱ��t�ı仯���±���ʾ(����NO2��N2O4��ת��)
2NO(g) ��H= ��110 kJ��mol��1;25��ʱ����NO��O2�����ʵ���֮��Ϊ2:1������Է�Ӧ�������ò�ѹ���о��䷴Ӧ�Ľ����������ϵ����ѹǿp��ʱ��t�ı仯���±���ʾ(����NO2��N2O4��ת��)
t/min | 0 | 80 | 160 | �� |
p/kpa | 75.0 | 63.0 | 55.0 | 55.0 |
0��80min,v(O2)=_______kpa/min����ѹǿ����Ũ�����õ���ƽ�ⳣ����K(p)��ʾ��25��ʱ��K(p)��ֵΪ___________(����3λ��Ч����)��
���𰸡�0.004mol/��L��min�� ���� 4Fe��0H��2+02+2H2O=4Fe��0H��3 = -740 kJ/mol 0.15 3.20
��������
(1) ����![]() ����v(Fe2+)��
����v(Fe2+)��
(2) ����������������������������������Ksp[Fe(OH)3]��2.5��10��39�� Ksp[Fe(OH)2]��1.0��10��15����c( Fe2+) /c(Fe3+)��
(3)���ø�˹���ɼ���aֵ��
(4) v(O2)=![]() �����á�����ʽ������K(p)��
�����á�����ʽ������K(p)��
(1)����ͼʾ����pH��5.5�Ļ����£��÷�Ӧ��0��15min��Fe2+��Ũ�ȱ仯��0.1mol/L��60%=0.06 mol/L��v(Fe2+)=![]() 0.004mol/��L��min��������ͼʾ��������ҺpH��Fe2+��������������
0.004mol/��L��min��������ͼʾ��������ҺpH��Fe2+��������������
(2)�ڶ����� ��������������������Ϊ����������4Fe��OH��2+O2+H2O=4Fe��OH��3����Ӧ�ﵽƽ��״̬ʱ��![]() =
= ![]() =
=![]() �� PH=13ʱc��OH-��=
�� PH=13ʱc��OH-��=![]() mol/L=10-1mol/L��
mol/L=10-1mol/L�� ![]() =
=![]() =4.0��1022��
=4.0��1022��
(3) NO(g)��H2O(g)�ı�Ħ�������ʷֱ�Ϊ+90kJ/mol��-280 kJ/mol����
��![]() N2(g)+
N2(g)+ ![]() O2(g)= NO(g) ��H= +90kJ/mol ��
O2(g)= NO(g) ��H= +90kJ/mol ��
��H2(g)+ ![]() O2(g)= H2O(g) ��H= -280 kJ/mol��
O2(g)= H2O(g) ��H= -280 kJ/mol��
���ݸ�˹���ɢڡ�2-�١�2��2NO(g)+2H2(g) ==N2(g)+2H2O(g): ��H��a= -740 kJ/mol��
(4) v(O2)=![]() =
=![]() 0.15 kpa/min��
0.15 kpa/min��
����160minʱ�ﵽƽ�⣬
2NO��g��+O2��g���T2NO2��g��
��ʼ 2nn 0
ת�� 2xx2x
ƽ�� 2n-2xn-x2x
![]() =
=![]() �����x=0.8n��
�����x=0.8n��
��ѹǿ����Ũ�����õ���ƽ�ⳣ����K��p����ʾ��25��ʱ��K��p����ֵΪ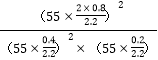 =3.20��
=3.20��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪ij�¶��£�Ksp��AgCl����1.56��10-10 mol2��L-2��Ksp��Ag2CrO4����1��10-12 mol3��L-3������������ȷ����
A. ����AgCl��Һ�뱥��Ag2CrO4��Һ��ȣ�ǰ�ߵ�c��Ag+����
B. ���Ȼ�������Һ�м����Ȼ�����Һ���Ȼ�����Ksp��С
C. ��0.0008 mol/L��K2CrO4��Һ�м���������0.002 mol/L AgNO3 ��Һ����CrO42 -��ȫ����
D. ��0.001mol/L��AgNO3 ��Һ����0.001 mol/L KCl��0.001 mol/L K2CrO4�Ļ����Һ�У����Ȳ���AgCl����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25��ʱ����c(HA)+c(A-)=0.1mol/L ��һ��HA��KA �����Һ����Һ��c(HA)��c(A-)��pH�Ĺ�ϵ����ͼ��ʾ��������������ȷ����

A. pH= 5.75 ����Һ��: c(K+)>c(A- )>c(HA)>q(H+)>c(OH- )
B. ����W ����ʾ��Һ����ʼ������ҺӦ����c(HA)+c(A-)=0.1mol/L ��c(KA)
C. pH=3.75����Һ�У�c(K+)+c(H+)-c(OH-)+c(HA)=0.1mol/L
D. ��A-��ˮ�ⳣ��ΪKb ��lgKb=-9.25
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25��ʱ����Ũ�Ⱦ�Ϊ0.1molL������ֱ�ΪVa��Vb��HX��Һ��NH3��H2O��Һ����ͬ����Ȼ�ϣ�����Va+Vb��100mL��Va��Vb����Һ��pH�Ĺ�ϵ��ͼ��ʾ������˵����ȷ����( )

A. Ka(HX)>Kb(NH3��H2O)
B. b��ʱc(NH4+)>c(HX)>c(OH��)��c(H+)
C. a��b��d�����У�ˮ�ĵ���̶�d>b>a
D. a ��b������У����ܴ���c(X��)<c(NH4+)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������кͷ�Ӧ��Ӧ�ȵIJⶨ�����������¡����������£���ʢ��20mL2.08mol/L��NaOH��Һ���Թ��з���ι�����5 mLδ֪Ũ�ȵ�H2SO4��Һ(�ӱ���ÿ�μ���1 mL)�����Һ���¶ȷֱ���21.4�桢22.5�桢24.2�桢25.2�桢25.18�棬���������Һ�����ʵ���Ũ��Լ��( )
A. 20.8 mol/L B. 5.2 mol/L C. 6.9 mol/L D. 4.16 mol/L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ˮ�����ǹ�ϵ���ཡ������Ҫ���⡣
��1��Cl2��������������ˮ���������ʣ�д��Cl2����ˮ������Ӧ�����ӷ���ʽ��___��
��2��ClO2��һ�ָ�Ч���Ͷ�������������ȡ��Cl2��Ϊ��������ˮ������������ҵ����KClO3��Na2SO3��H2SO4�������Ƶ�ClO2���÷�Ӧ���������뻹ԭ�����ʵ���֮��Ϊ____��
��3���������(K2FeO4)��һ�����͡���Ч�����ˮ����������Cl2��ClO2�����Ը�ǿ����������Ⱦ����ɫˮ����������ҵ�����Ƶø������ƣ�Ȼ���ڵ����£������������Һ�м���KOH�����;Ϳ�����������ء���������Ϣ��֪����ͬ�����£����������ܽ�ȱȸ�������ܽ��__(������������С��)�������������ˮ�ų���������ɱ������������������ˮ��������������������塣��һ�����ӷ���ʽ��ʾ������ش���ˮ�Ĺ���____���ɷ��Ʊ��������Ƶ���Ҫ��ӦΪ2FeSO4��6Na2O2===2Na2FeO4��2Na2O��2Na2SO4��O2�����÷�Ӧ�Ļ�ԭ����___��ÿ����1molNa2FeO4ת��__mol���ӡ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����˺��ʳ��ˮ�Ժ��п����Ե�CaCl2��MgCl2��Na2SO4�����ʣ�ͨ�����¼���ʵ�鲽�裬���Ƶô�����ʳ��ˮ���ټ����Թ�����BaCl2��Һ���ڼ����Թ�����NaOH��Һ���ۼ����Թ�����Na2CO3��Һ���ܵ���ϡ�����������ݲ������ݹ��ˡ���ȷ�IJ���˳����
A.�٢ڢۢݢ�B.�ۢڢ٢ݢ�C.�ڢ٢ۢܢ�D.�ۢݢڢ٢�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ȤС����Ƴ���ͼ��ʾװ�����Ľ��̲�����ͭ�����ᷴӦ��ʵ�飬��̽����ѧʵ�����ɫ����

��1��ʵ��ǰ���رջ���b���Թ�d�м�ˮ����û�����ܿڣ������Թ�c��d�Ľ���������c����Ŀ����_________________________________��
��2����d�м�����NaOH��Һ��c�з�һС��ͭƬ���ɷ�Һ©��a��c�м���2 mLŨ���ᣬc�з�Ӧ�Ļ�ѧ����ʽ��______________________________________��
��3���±�����ȡ����ͭ�����ַ�������������ɫ��ѧ�������ѷ�����__________��
���� | ��Ӧ�� |
�� | Cu��ŨHNO3 |
�� | Cu��ϡHNO3 |
�� | Cu��O2��ϡHNO3 |
��4����С�黹������װ�ý���ʵ��֤�����ԣ�HCl��H2CO3��H2SiO3�����Һ©��a�м�����Լ���___________��c�м�����Լ���_________��d�м�����Լ���_________��ʵ������Ϊ_______________________��
����ʵ����ڲ���֮�����Ľ��Ĵ�ʩ��___________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������Ͻ���һ����Ҫ��������ϡ�ij����С���������ԭ�� NH4VO3��TiO2�� Fe2O3���Ƴ���VO2+��TiO2+�� Fe3+�Ľ�������Һ��Ȼ��ѡ��ˮ�����������й�������Ӧ���Թ�������[��VO(OH)2��Ti(OH)4��Fe(OH)3]�������ջ�ԭ�Ʊ��Ͻ���Ʒ���Ʊ����������װ������ͼ��

��1��ʵ������Ũ��ˮ����500mL2 mol��L��1��ϡ��ˮ�����õ��IJ����������ձ�����ͷ�ιܺ�___��____��____��
��2��װ��B��������_________��
��3���Ʊ�VO2+ʱ���ò��ὫVO2+��ԭ��VO2+�����Ѳ����Ϊ���ᣬҲ�ܵõ�VO2+���������һ���ж����壬�÷�Ӧ�����ӷ���ʽΪ___________��
��4����Ӧ����������¶�Ϊ60����������ƿ�ļ��ȷ�ʽ��________��
��5����������ƿ�еμӺ��������ӵĻ��Һ��������Һ��ȡ����ֳ�����
������ϲ���Һ�Ƿ�Fe3+��ʵ�鷽����_______________��
�������ˡ���ˮ�Ҵ�ϴ�ӡ����¸���ù������ʹ����ˮ�Ҵ�ϴ�ӵ��ŵ���_______��
��6������5�����ù���������ղ���ԭ��÷���������Ͻ�Ϊ�ⶨ��Ʒ����������������ȡ50.60g��Ʒ��������ϡ���ᣨ����V��Ti���ܣ������ˣ�����Һ���250.00mL��ȡ25.00mL��Һ����0.1000mol��L��1 ����KMnO4��Һ�ζ�������ƽ��ʵ���ƽ������KMnO4��Һ�����Ϊ20.00 mL�����Ʒ��������������Ϊ________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com