
| A. | CH4、C2H4 | B. | C2H6、C3H6 | C. | CH4、C2H6 | D. | C2H6、C2H2 |
分析 常温常压下水为液态,设烃的混合物的平均化学式为CxHy,在氧气中燃烧的化学方程式为CxHy+(x+$\frac{y}{4}$)O2$\stackrel{点燃}{→}$xCO2+$\frac{y}{2}$H2O(l),根据体积变化利用差量法计算,然后根据计算结果进行判断,以此来解答.
解答 解:设混合烃的平均组成为CxHy,则:
CxHy+(x+$\frac{y}{4}$)O2$\stackrel{点燃}{→}$xCO2+$\frac{y}{2}$H2O(l)△V
1 1+$\frac{y}{4}$
amL 2amL
则:1+$\frac{y}{4}$=2,
解得:y=4,
即混合气体分子中平均含有4个H原子即可,D按照1:1混合满足平均含有4个H原子,但不符合任意比,B、C中H平均个数均大于4,
由于是按任意比例混合,则每种有机物分子中都含有4个H,
则满足条件的只有A,
故选A.
点评 本题考查混合物反应的计算,为高频考点,题目难度中等,明确烃的燃烧通式及差量法在化学计算中的应用为解答关键,试题侧重考查学生的分析、理解能力及化学计算能力.


科目:高中化学 来源: 题型:选择题
| A. | 原子晶体中只存在非极性共价键 | |
| B. | 在氯化钠晶体中每个Na+(或Cl-)周围都紧邻8个Cl-(Na+) | |
| C. | 离子晶体在熔化时,离子键被破坏 | |
| D. | 熔融状态下导电的晶体一定是金属晶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题

查看答案和解析>>
科目:高中化学 来源: 题型:实验题
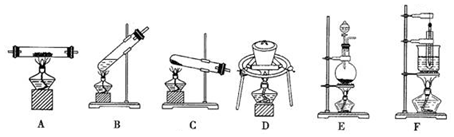
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{w(A+x-n)}{A}$mol | B. | $\frac{A(A-x+n)}{w}$mol | C. | $\frac{w(A-x-n)}{A}$mol | D. | $\frac{w(A+x+n)}{A}$mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将表面变暗的金属钠粒投入干燥氯气中,无明显现象 | |
| B. | 将在空气中点燃的金属钠伸入干燥氯气中会继续燃烧,产生黄色火焰和大量黄烟 | |
| C. | 将SO2气体通入溴水中使溴水褪色,滴加BaCl2溶液有白色沉淀产生 | |
| D. | SO2气体通入品红溶液中,品红褪色,加热所得无色溶液红色复原 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | a=2,b=1 | B. | a=3,b=2 | C. | a=2,b=2 | D. | a=3,b=3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 阳离子 | Mg2+ | Fe2+ | Fe3+ |
| 开始沉淀 | 9.1 | 7.6 | 1.9 |
| 完全沉淀 | 11.1 | 9.7 | 3.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 现象或事实 | 解释 |
| A | 碱性锌锰电池比普通锌锰电池性能好 | 锌在碱性介质中被氧化成更高价态 |
| B | 施肥时,草木灰(有效成分为K2CO3)不能与铵盐氮肥混合使用 | 它们反应生成氨气会降低肥效 |
| C | 配制FeCl2溶液时加入少量铁粉 | 抑制Fe2+的水解 |
| D | 纯水和干木头都不导电,但木头用水浸湿后却可以导电 | 水和干木头的某些成分发生化学反应 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com