
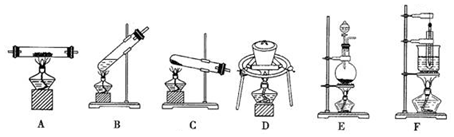
分析 (1)试管、坩埚、蒸发皿可直接加热,烧杯、烧瓶须垫石棉网加热,F为水浴加热,可提高稳定的加热环境;
(2)H2还原CuO,所选装置应有进气和出气装置;
(3)NH4Cl与Ca(OH)2混合制NH3应在试管中加热进行;
(4)加热固体,应在坩埚中进行.
(5)MnO2与浓盐酸混合制氯气,应在加热条件下,在烧瓶中进行.
解答 解:(1)试管、坩埚、蒸发皿可直接加热,烧杯、烧瓶须垫石棉网加热,F为水浴加热,可提高稳定的加热环境,使仪器受热均匀,便于控制KNO3溶液的温度,
故答案为:石棉网;水浴加热;使仪器受热均匀,便于控制KNO3溶液的温度;
(2)H2还原CuO,所选装置应有进气和出气装置,A符合,故答案为:A;
(3)NH4Cl与Ca(OH)2混合制NH3应在试管中加热进行,为固体和固体反应生成气体,试管口应略朝下,C符合,故答案为:C;
(4)加热固体,应在坩埚中进行,故答案为:D;
(5)MnO2与浓盐酸混合制氯气,应在加热条件下,在烧瓶中进行,E符合,若该装置只加热液体时,为防止液体暴沸,容器内必须放碎瓷片或沸石,
故答案为:E;碎瓷片或沸石.
点评 本题考查较为综合,涉及气体的制备和仪器的使用,为高频考点,侧重学生的基础知识和基本技能的考查,注意把握实验原理和实验基本操作,难度不大.


科目:高中化学 来源: 题型:选择题
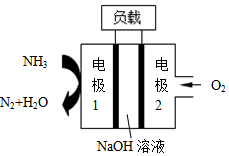 瑞典ASES公司设计的曾用于驱动潜艇的液氨-液氧燃料电池示意图如图,下列有关说法正确的是( )
瑞典ASES公司设计的曾用于驱动潜艇的液氨-液氧燃料电池示意图如图,下列有关说法正确的是( )| A. | 电池工作时,Na+向电极1移动 | |
| B. | 电池工作时电极2附近溶液的pH减小 | |
| C. | 电池总反应为:4NH3+3O2=2N2+6H2O | |
| D. | 电极1发生的电极反应为:2NH3-6e-=N2+6H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 化学键 | H-H | H-Cl | H-Br | H-I |
| 键能KJ•mol-1 | 436.0 | 431.8 | 366 | 298.7 |
| A. | 氢气 | B. | 氯化氢 | C. | 溴化氢 | D. | 碘化氢 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①⑤ | B. | ①②③ | C. | ①③④⑤ | D. | ②③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用锌与稀硫酸反应制备氢气时,加入少量硫酸铜 | |
| B. | Al与稀硫酸反应制取H2时,改用质量分数为98.3%的浓硫酸 | |
| C. | Fe与稀硫酸反应时,把铁粉改为铁片 | |
| D. | Na与水反应时增大水的用量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 大部分药物都有毒副作用,应该在医生指导下使用 | |
| B. | 无矾油条克服了传统油条中因添加明矾,导致铝过多摄入,损害脑细胞的问题 | |
| C. | 氢化油也被叫做“植物奶油”,广泛用于食品焙烤领域,既美味又健康 | |
| D. | 塑化剂风波中,不法商贩用工业塑化剂替代乳化剂添加在饮料中,对人体有害 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH4、C2H4 | B. | C2H6、C3H6 | C. | CH4、C2H6 | D. | C2H6、C2H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 电解硫酸钠溶液联合生产硫酸和烧碱溶液的装置如图所示,其中阴极和阳极均为惰性电极.测得同温同压下,气体甲与气体乙的体积比约为1:2,以下说法不正确的是( )
电解硫酸钠溶液联合生产硫酸和烧碱溶液的装置如图所示,其中阴极和阳极均为惰性电极.测得同温同压下,气体甲与气体乙的体积比约为1:2,以下说法不正确的是( )| A. | a极与电源的正极相连 | |
| B. | 产物丙为硫酸溶液 | |
| C. | 离子交换膜d为阳离子交换膜(允许阳离子通过) | |
| D. | a电极反应式为2H++2e-═H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com