
 电解硫酸钠溶液联合生产硫酸和烧碱溶液的装置如图所示,其中阴极和阳极均为惰性电极.测得同温同压下,气体甲与气体乙的体积比约为1:2,以下说法不正确的是( )
电解硫酸钠溶液联合生产硫酸和烧碱溶液的装置如图所示,其中阴极和阳极均为惰性电极.测得同温同压下,气体甲与气体乙的体积比约为1:2,以下说法不正确的是( )| A. | a极与电源的正极相连 | |
| B. | 产物丙为硫酸溶液 | |
| C. | 离子交换膜d为阳离子交换膜(允许阳离子通过) | |
| D. | a电极反应式为2H++2e-═H2↑ |
分析 装置图分析可知是电解装置,电极硫酸钠溶液,实质是电解水,气体甲与气体乙的体积比约为1:2,气体甲为氧气,气体乙为氢气,阳极生成氧气,电极反应4OH--4e-=2H2O+O2,阴极生成氢气,2H++2e-=H2↑,气体体积比为1:2,所以判断a电极是阳极,b电极是阴极,在阳极室得到硫酸,在阴极室得到氢氧化钠,则c为阴离子交换膜,d为阳离子交换膜.
解答 解:A、根据分析可知a电极为阳极,与电源正极相连,故A正确;
B、阳极a生成氧气,电极反应4OH--4e-=2H2O+O2↑,阳极室水的 电离平衡被破坏生成氢离子,生成产物丙为硫酸,故B正确;
C、阳极a生成氧气,电极反应4OH--4e-=2H2O+O2↑,阳极室水的 电离平衡被破坏生成氢离子,生成产物丙为硫酸,阴极生成氢气,2H++2e-=H2↑,生成产物丁为氢氧化钠,则c为阴离子交换膜,d为阳离子交换膜,故C正确;
D、阳极a生成氧气,电极反应4OH--4e-=2H2O+O2↑,故D错误;
故选D.
点评 本题考查了电解原理的分析应用,电极产物和电极名称判断是解题关键,题目难度中等,侧重于考查学生对电解知识的综合应用能力.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | S(s,单斜)═S(s,正交)△H3<0,正交硫比单斜硫稳定 | |
| B. | 单斜硫转化为正交硫的反应是吸热反应 | |
| C. | △H3=+0.33 kJ•mol-1 | |
| D. | S(s,单斜)═S(s,正交)△H3>0,单斜硫比正交硫稳定 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
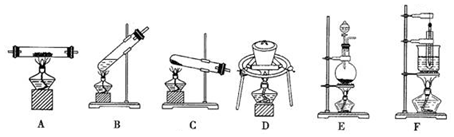
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将表面变暗的金属钠粒投入干燥氯气中,无明显现象 | |
| B. | 将在空气中点燃的金属钠伸入干燥氯气中会继续燃烧,产生黄色火焰和大量黄烟 | |
| C. | 将SO2气体通入溴水中使溴水褪色,滴加BaCl2溶液有白色沉淀产生 | |
| D. | SO2气体通入品红溶液中,品红褪色,加热所得无色溶液红色复原 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | a=2,b=1 | B. | a=3,b=2 | C. | a=2,b=2 | D. | a=3,b=3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 阳离子 | Mg2+ | Fe2+ | Fe3+ |
| 开始沉淀 | 9.1 | 7.6 | 1.9 |
| 完全沉淀 | 11.1 | 9.7 | 3.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
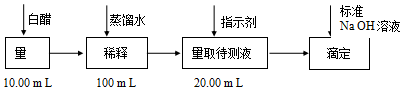
| 实验次数 | 稀释后白醋 体积(mL) | 标准NaOH溶液 | ||
| A | B | 消耗体积(mL) | ||
| 1 | 20.00 | 22.05 | ||
| 2 | 20.00 | 21.34 | ||
| 3 | 20.00 | 21.30 | ||
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,5.6 LNO和5.6LO2混合后的分子总数为0.5 NA | |
| B. | 1mol乙烷分子含有8NA个共价键 | |
| C. | 58.5 g氯化钠固体中含有NA个氯化钠分子 | |
| D. | 标准状况下,22.4L氯气与足量氢氧化钠溶液反应转移的电子数为NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com