
| 化学键 | N-H | N-N | O═O | N≡N | O-H |
| 键能 (kJ•mol-1) | 386 | 167 | 498 | 946 | 460 |
分析 (1)先写出化学方程式N2H4+O2═N2+2H2O,然后根据焓变=反应物的总键能-生成物的总键能计算焓变,再根据化学方程式计算1mol肼完全燃烧时放出的热量;
(2)肼-空气燃料电池放电时,负极上肼失电子和氢氧根离子反应生成H2O和氮气,正极上氧气得电子和水反应生成氢氧根离子,据此分析解答;
(3)N60分子中每个N原子均以氮氮单键结合三个氮原子,且N60结构中每个氮原子均形成8个电子的稳定结构,每个N-N键为一个N原子提供$\frac{1}{2}$;
解答 解:(1)N2H4燃烧的化学方程式为N2H4(g)+O2(g)═N2(g)+2H2O(g),△H=反应物的总键能-生成物的总键能=167 kJ•mol-1+386 kJ•mol-1×4+498 kJ•mol-1-946 kJ•mol-1-460 kJ•mol-1×4=-577 kJ•mol-1,N2H4燃烧的热化学方程式为N2H4(g)+O2(g)═N2(g)+2H2O(g)△H=-577 kJ•mol-1,所以1mol肼完全燃烧时放出的热量为577 kJ,
故答案为:577kJ;
(2)肼-氧气碱性燃料电池中,负极上燃料肼失电子和氢氧根离子反应生成水和氮气,电极反应式为N2H4+4OH--4e-=4H2O+N2↑,正极发生还原反应,电极方程式为O2+2H2O+4e-=4OH-,
故答案为:O2+2H2O+4e-=4OH-;
(3)N60分子中每个N原子均以氮氮单键结合三个氮原子,且N60结构中每个氮原子均形成8个电子的稳定结构,每个N-N键为一个N原子提供$\frac{1}{2}$,则1个N60分子的结构中含有N-N数目为60×3×$\frac{1}{2}$=90,
故答案为:90;
点评 本题考查了化学反应的能量变化与反应的焓变关系、原电池和电解池原理及物质的量的计算,根据各个电极上得失电子书写电极反应、物质结构特征分析,注意反应热与键能以及化学计量数间的关系和分子结构的分摊法计算化学键数,题目难度中等.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
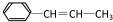 ,它可能具有的性质是( )
,它可能具有的性质是( )| A. | 可以发生加成、取代、氧化反应 | |
| B. | 能使溴水褪色,但不能使酸性高锰酸钾褪色 | |
| C. | 能发生加聚反应,其生成物可用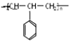 来表示 来表示 | |
| D. | 易溶于水,也易溶于有机溶剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 由于水中存在氢键,所以水很稳定 | |
| B. | 能与酸反应生成盐和水的氧化物一定是碱性氧化物 | |
| C. | 单质分子中一定含有共价键 | |
| D. | 由非金属元素组成的化合物不一定是共价化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子核内有 10 个中子的氧原子:${\;}_{8}^{16}$O | |
| B. | 氢氧根离子的电子式: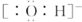 | |
| C. | 基态 Cr 的价电子排布式为:3d44s2 | |
| D. | 某元素原子的电子排布图: |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaOH的电子式: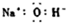 | B. | I4O9(碘酸碘)中碘的化合价为+3,+5 | ||
| C. | NH5的结构式为: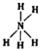 | D. | CO2的比例模型: |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | N2、H2、NH3的百分含量相等 | |
| B. | 单位时间,消耗a mol N2的同时消耗3mol H2 | |
| C. | 单位时间,消耗a molN2的同时生成3a mol H2 | |
| D. | 反应若在定容的密器中进行,压强为反应前的一半 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
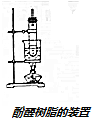 某课外活动小组结合一下材料制酚醛树脂,用苯酚和甲醛为原料,在酸或碱的催化作用下缩聚而成,苯酚过量,在酸性催化剂作用下,缩聚成线型结构的热塑性酚醛树脂,甲醛过量,在碱性催化剂作用下,缩聚成体型结构的热固性酚醛树脂设计实验如下:
某课外活动小组结合一下材料制酚醛树脂,用苯酚和甲醛为原料,在酸或碱的催化作用下缩聚而成,苯酚过量,在酸性催化剂作用下,缩聚成线型结构的热塑性酚醛树脂,甲醛过量,在碱性催化剂作用下,缩聚成体型结构的热固性酚醛树脂设计实验如下: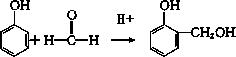
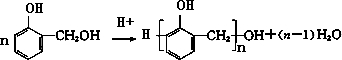
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
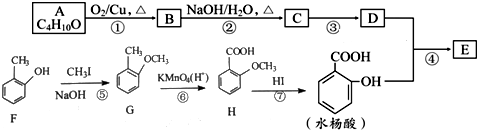
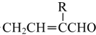
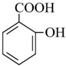 →
→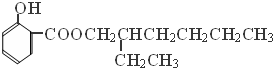 +H2O;
+H2O;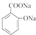
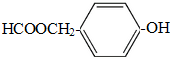 (写结构简式).
(写结构简式).查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com