
【题目】将 4 mol A 气体和 2 mol B 气体在 2 L 的定容容器中混合并在一定条件下发生如下反应:2A(g)+B(g)![]() 2C(g) △H<0 ,经 2 s(秒)后测得 C 的浓度为 0. 6 mol·L-1 ,现有下列几种说法:①用物质 A 表示的反应的平均速率为 0.3 mol·L-1s-1;②达到平衡状态时,升高温度,平衡逆向移动,化学平衡常数K减小;③2 s 时物质 A 的转化率为70% ;④达平衡时,增加A物质的量,平衡正向移动,A的转化率降低;⑤当B和C的生成速率相等时,该反应达到平衡状态。其中不正确的是( )
2C(g) △H<0 ,经 2 s(秒)后测得 C 的浓度为 0. 6 mol·L-1 ,现有下列几种说法:①用物质 A 表示的反应的平均速率为 0.3 mol·L-1s-1;②达到平衡状态时,升高温度,平衡逆向移动,化学平衡常数K减小;③2 s 时物质 A 的转化率为70% ;④达平衡时,增加A物质的量,平衡正向移动,A的转化率降低;⑤当B和C的生成速率相等时,该反应达到平衡状态。其中不正确的是( )
A.①③B.②⑤C.③⑤D.②③
【答案】C
【解析】
根据题干数据,利用三段法进行计算。
2A(g) + B(g)![]() 2C(g)
2C(g)
始(mol/L) 2 1 0
转(mol/L) 0.6 0.3 0.6
2s(mol/L) 1.4 0.7 0.6
①反应的平均速率等于浓度的变化量与时间的变化量的比值,因此用物质 A 表示的平均反应速率v==![]() =0.3 mol·L-1s-1,正确;
=0.3 mol·L-1s-1,正确;
②该反应为放热反应,升高温度,平衡逆向移动,化学平衡常数K减小,正确;
③2 s 时物质 A 的转化率=![]() ×100%= 30%,错误 ;
×100%= 30%,错误 ;
④达平衡时,增加A物质的量,平衡正向移动,A的转化率降低,正确;
⑤B和C的生成速率之比为1:2,不相等,不是平衡状态,错误;
不正确的是③⑤;
答案选C。


 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案科目:高中化学 来源: 题型:
【题目】下列有关铜与过量浓硫酸反应的实验说法不正确的是( )
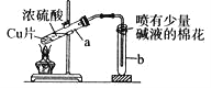
A.喷有碱液的棉花是为了防止 SO2 污染环境
B.将水注入反应后冷却的试管 a 中,溶液变为蓝色
C.SO2 能使 KMnO4 水溶液褪色
D.反应的化学方程式是 Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙酸乙酯是重要的有机物。某化学兴趣小组对乙酸乙酯的制取进行探究活动。
[查阅资料]乙酸乙酯:无色、有芬芳气味的液体,沸点77℃,熔点-83.6℃,密度0.901g/cm3,溶于乙醇、氯仿、乙醚和苯等,微溶于水,在饱和碳酸钠中溶液溶解度更小,比水轻。

[反应原理]
CH3COOH+CH3CH2OH![]() CH3COOC2H5+H2O
CH3COOC2H5+H2O
[实验探究]某化学兴趣小组设计如图装置进行实验。在大试管a内加入碎瓷片后,加入10mL乙醇,边振荡边加入5mL98%的浓H2SO4,冷却后再加入8mL冰醋酸,点燃酒精灯缓慢加热,将产生的蒸气经导管通入到试管b中的的饱和Na2CO3溶液的液面上,观察现象。
[问题讨论]
(1)试管a内加入碎瓷片的作用_______(填“防止暴沸”或“防止倒吸”);
(2)试管b中长导管没有伸入饱和Na2CO3溶液的原因是_______(填“防止暴沸”或“防止倒吸”);
(3)实验中饱和碳酸钠溶液的作用是_______________;
A.中和乙酸和乙醇
B.加速酯的生成,提高其产率
C.溶解乙醇,中和乙酸,降低乙酸乙酯的溶解,有利于分层析出。
(4)反应结束后试管b中的现象是_______;
A.溶液不分层
B.溶液分层,无色油状液体在上层
C.溶液分层,无色油状液体在下层
(5)若用9.2g乙醇与足量的冰醋酸反应,分离得到纯乙酸乙酯13.2g,反应的产率是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】胆矾 CuSO4·5H2O 可写[Cu(H2O)4]SO4·H2O,其结构示意图如图:
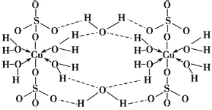
下列有关胆矾的说法正确的是( )
A.Cu2+的电子排布式为[Ar]3d84s1
B.胆矾是分子晶体,分子间存在氢键
C.氧原子参与形成离子键、配位键和氢键三种化学键
D.因为作用力的不同,胆矾中的水在不同温度下会分步失去
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.现有常温下浓度均为![]() 的下列四种溶液:
的下列四种溶液:![]() 溶液
溶液![]() 溶液
溶液![]() 溶液
溶液![]() 溶液
溶液![]() 溶液。
溶液。
(1)这5种溶液pH由大到小的顺序是______,其中由水电离的H+浓度最小的是______。(填序号)
(2)②中各离子浓度由大到小的顺序是______,![]() 的水解平衡常数
的水解平衡常数![]() ______。
______。![]() 已知碳酸的电离常数
已知碳酸的电离常数![]() ,
,![]()
(3)向③中通入少量氨气,此时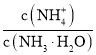 的值______(填“增大”、“减小”或“不变”)。
的值______(填“增大”、“减小”或“不变”)。
(4)若将③和④混合后溶液恰好呈中性,则混合前③的体积______ ④的体积(填“大于”、“小于”或“等于”)。
(5)将②③④的溶液分别蒸干并灼烧,最终可得原溶质的是______(填序号)。
(6)100mL3mol/LH2SO4溶液与足量的Zn反应,为减缓产生的H2速率但又不影响H2的总量,可采取的措施是______(填字母)。
A.加![]() 固体 B.加
固体 B.加![]() 固体 C.加
固体 C.加![]() 溶液 D.加氨水 E.加
溶液 D.加氨水 E.加![]() 溶液
溶液
II.常温下,向![]() 溶液中加入
溶液中加入![]() 溶液,可观察到的现象是______,发生反应的离子方程式为______,若将所得悬浊液的pH值调整为4,则溶液中
溶液,可观察到的现象是______,发生反应的离子方程式为______,若将所得悬浊液的pH值调整为4,则溶液中![]() 的溶液为______mol/L (已知常温下
的溶液为______mol/L (已知常温下![]() 。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素X、Y、Z在周期表中的位置如图。下列说法正确的是
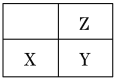
A. Z元素的最高化合价一定大于X元素
B. 三种元素原子半径由高到低的顺序一定是Y>X>Z
C. 若它们的原子最外层电子数之和为11,则X为金属元素
D. 若它们均为金属元素,则Y的最高价氧化物对应水化物的碱性最强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Al 的晶体中原子的堆积方式如图甲所示,其晶胞特征如图乙所示。

已知 Al的原子半径为 d,NA代表阿伏加德罗常数,Al 的相对原子质量为 M。
(1)晶胞中 Al 原子的配位数为_____,一个晶胞中 Al 原子的数目为_____,该晶胞的空间利用率是_____。
(2)该晶体的密度为_____(用字母表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】香豆素﹣4是一种激光染料,应用于可调谐染料激光器。香豆素﹣4由C、H、O三种元素组成,分子球棍模型如图所示,下列有关叙述正确的是( )
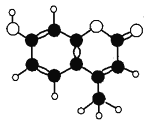
① 分子式为C10H9O3 ② 能与Br2水发生取代反应
③能与Br2水发生加成反应 ④能使酸性KMnO4溶液褪色
⑤ 1mol香豆素﹣4最多能与2molNaOH的溶液反应
A.①②③B.③④⑤C.②③④D.②③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,H2A和H2NCH2CH2NH2溶液中各组分的物质的量分数δ随pH的变化如图(I)、(II)所示。下列说法不正确的是已知:![]() 。
。
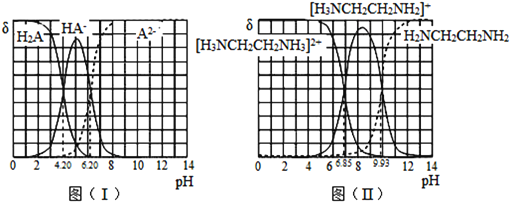
A.NaHA溶液中各离子浓度大小关系为:![]()
B.乙二胺(H2NCH2CH2NH2)的Kb2=10-7.15
C.[H3NCH2CH2NH3]A溶液显碱性
D.向[H3NCH2CH2NH2] HA溶液中通人HCl,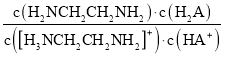 不变
不变
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com