
| A.加入HNO3将Fe2+氧化成Fe3+,再加水稀释至pH4-5 |
| B.向溶液中通入Cl2,再加入CuO粉末调节至pH4-5 |
| C.向溶液中通入Cl2,在通入NH3调节至pH4-5 |
| D.向溶液中通入H2O2, 再加入CuO粉末调节至pH4-5 |
科目:高中化学 来源:不详 题型:单选题
| A.残余固体可能为铁、铜混合物 | B.最后得到的溶液中含有Fe3+ |
| C.最后得到的溶液中只含Cu2+ | D.残余固体一定全部是铜 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题

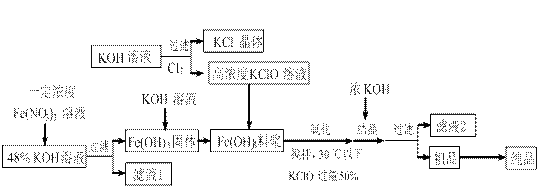
 ▲ 。
▲ 。 O3的混合溶液,经测定ClO-与ClO3-离子的物质的量之比是1:2,则Cl2与氢氧化钾反应时,被还原的氯元素和被氧化的氯元素的物质的量之比为 ▲ 。
O3的混合溶液,经测定ClO-与ClO3-离子的物质的量之比是1:2,则Cl2与氢氧化钾反应时,被还原的氯元素和被氧化的氯元素的物质的量之比为 ▲ 。
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.分别还原a mol Fe2O3所需H2、Al、CO物质的量之比为3 ∶2 ∶3 |
| B.铁在纯氧中燃烧或高温下和水蒸气反应均能得到Fe3O4 |
| C.工业上可用铁制容器储存、运输浓硝酸、浓硫酸 |
| D.检验某物质是否含Fe2O3的操作步骤为:样品→粉碎→加热→溶解→过滤→向滤液中加KSCN溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.使用硫酸过量 | B.使用铁屑过量 |
| C.使用稀硫酸 | D.使用浓硫酸 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com