
【题目】下列卤代烃在KOH醇溶液中加热不反应的是( )
①C6H5Cl ②(CH3)2CHCH2Cl ③(CH3)3CCH2Cl ④CHCl2﹣CHBr2 ⑤ ![]() ⑥CH2Cl2 .
⑥CH2Cl2 .
A.①③⑥
B.②③⑤
C.全部
D.②④
【答案】A
【解析】①有机物发生消去反应发生后将会形成不饱和键,而氯苯中相邻的碳原子是苯环的一部分,没有氢原子,故不能发生消去反应,故①符合题意;
②和氯相连的碳的相邻碳原子上有氢,故能消去,生成对应的烯烃和氯化钾,故②不符合题意;
③和氯相连的碳的相邻碳原子上没有氢,所以不能发生消去反应.故③符合题意;
④和氯或溴相连的碳相邻碳原子上有氢,故能消去,生成对应的烯烃或炔烃和氯化钾,故④不符合题意;
⑤和溴相连的碳上有氢,故能发生消去反应,生成对应的烯烃和溴化钾,故⑤不符合题意;
⑥二氯甲烷只有一个碳,没有相邻的碳,所以不能发生消去反应.故⑥符合题意;
所以答案是:A.
【考点精析】解答此题的关键在于理解卤代烃简介的相关知识,掌握卤代烃是烃分子中的氢原子被卤原子取代后的产物.


科目:高中化学 来源: 题型:
【题目】已知碳碳单键可绕键轴自由旋转,某烃的结构简式如图所示,下列说法中正确的是
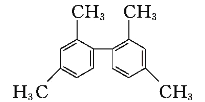
A. 该物质所有原子均可共面
B. 分子中至少有10个碳原子处于同一平面上
C. 分子中至少有11个碳原子处于同一平面上
D. 该有机物苯环上的一溴代物有6种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,已知醋酸的电离常数Ka=1.6×10-5,醋酸银的溶度积Ksp(CH3COOAg)=3.7×10-3。下列有关说法正确的是
A. 醋酸溶液中,c(CH3COO-)>c(H+)>c(OH-)
B. 将相同浓度的CH3COOH溶液与CH3COO Na溶液等体积混合,所得溶液呈碱性
C. 该温度下,1mol/L的醋酸溶液中,醋酸的电离度为0.4%
D. 该温度下,浓度均为0.02mol/L的CH3COONa溶液和AgNO3溶液等体积混合(忽略混合后溶液体积的变化),有CH3COOAg沉淀生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】香叶醇是合成玫瑰香油的主要原料,其结构简式如图所示:下列有关香叶醇的叙述正确的是( )
A.香叶醇的分子式为C10H18O
B.不能使溴的四氯化碳溶液褪色
C.不能使酸性高锰酸钾溶液褪色
D.能发生加成反应不能发生取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】席夫碱类化合物G有机合成、药物、新材料等方面有广泛应用。合成G的一种路线如下:
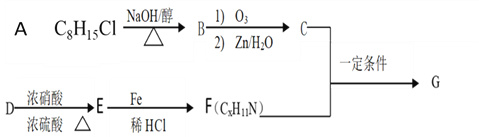
①![]()
②1molB经上述反应可生成2molC,且C不能发生银镜反应
③D属于单取代芳烃,其相对分子质量为106
④核磁共振氢谱显示F苯环上有两种化学环境的氢
⑤![]()
回答下列问题:
(1)B的化学名称_________________,A生成B的化学方程式___________________________________
(2)A 生成B , E 生成F的反应类型分别是__________,___________
C+F 生成G的化学方程式________________________________________________________________
(3)E的同分异构体中,含有苯环和氨基且能与碳酸氢钠反应生成CO2的共有_______种,其中核磁共振氢谱有五组峰,峰面积之比为1:2:2:2:2的结构简式为________________________(任意写一种)
(4)已知![]() 请以乙烯为原料,其他试剂任选,写出合成吸水材料聚丙烯酸钠的合成路线___________________________________________________________________________
请以乙烯为原料,其他试剂任选,写出合成吸水材料聚丙烯酸钠的合成路线___________________________________________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】尿黑酸是由酪氨酸在人体内非正常代谢而产生的一种物质.其转化过程如下:
下列说法错误的是( )
A.酪氨酸既能与盐酸反应,又能与氢氧化钠反应
B.1 mol尿黑酸与足量浓溴水反应,最多消耗3 mol Br2
C.对羟基苯丙酮酸分子中在同一平面上的碳原子至少有7个
D.1 mol尿黑酸与足量NaHCO3反应,最多消耗3 mol NaHCO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度时,向10mL.0.1mol/LCaCl2溶液中滴加0.1mol/L的Na2CO3溶液。滴加过程中溶液中-1gc(Ca2+)与Na2CO3溶液体积(V)的关系如图所示,下列有关说法正确的是( )
(已知1g5=0.7)

A. x、y两点c(Ca2+)之比为2000:3 B. Ksp(CaCO3)=5×10-9
C. w点对应的分散系很稳定 D. x、y、z三点中,水的电离程度最大的为x点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】废弃物回收利用可变废为宝。某工业固体废物的组成为Al2O3、FeO、Fe2O3等。下图是以该固体废物为原料制取氧化铝、磁性Fe3O4胶体粒子的一种工艺流程:

(1)检验制备Fe3O4胶体粒子成功的实验操作名称是____________________________。
(2)写出由溶液B制备磁性Fe3O4胶体粒子的离子方程式__________________________________。
(3)由溶液B制得Fe3O4胶体粒子的过程中,须持续通入N2。其原因是____________________________。
(4)向溶液C中加入NaHCO3溶液,溶液的pH_________(填“增大”,“不变”或“减小”)。
(5)固体D是Al(OH)3,空温时Al(OH)3溶于NaOH溶液反应的平衡常数等于20,则此时Al(OH)3![]() A1O2-+H++H2O的电离常数K=_______________。
A1O2-+H++H2O的电离常数K=_______________。
(6)用重路酸钾(K2Cr2O7)可测定产物磁性Fe3O4胶体粒子中铁元素的含量,过程如下图。已知,反应中K2Cr2O7被还原为Cr3+。

①写出甲→乙的化学方程式___________________________________。
②写出乙→丙的离子方程式_________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碘及其化合物在合成杀菌剂、药物等方面具有广泛用途.回答下列问题:
(1)大量的碘富集在海藻中,用水浸取后浓缩,再向浓缩液中加MnO2和H2SO4 , 即可得到I2 , 写出该反应的离子方程式 .
(2)一种碘和氧的化合物(I4O9),可以称为碘酸碘,则I4O9中碘元素的化合价是 .
A.﹣1
B.+1
C.+3
D.+5
(3)若IOH是两性化合物,写出IOH的酸式电离的电离方程式 .
(4)已知反应2HI(g)═H2(g)+I2(g)△H=+11kJmol﹣1 , 1mol H2(g)、1mol I2(g)分子中化学键断裂时分别需要吸收436kJ、151kJ的能量,则1mol HI(g)分子中化学键断裂时需吸收的能量为kJ.
(5)Bodensteins研究了下列反应:2HI(g)H2(g)+I2(g).在716K时,气体混合物中碘化氢的物质的量分数x(HI)与反应时间t的关系如表:
t/min | 0 | 20 | 40 | 60 | 80 | 120 |
x(HI) | 1 | 0.91 | 0.85 | 0.815 | 0.795 | 0.784 |
x(HI) | 0 | 0.60 | 0.73 | 0.773 | 0.780 | 0.784 |
①根据上述实验结果,该反应的平衡常数K的计算式为: .
②上述反应中,正反应速率为υ正=k正x2(HI),逆反应速率为υ逆=k逆x(H2)x(I2),其中k正、k逆为速率常数,则k逆为(以K和k正表示).
③由上述实验数据计算得到υ正~x(HI)和υ逆~x(H2)的关系可用如图表示.当升高到某一温度时,反应重新达到平衡,相应的点分别为(填字母).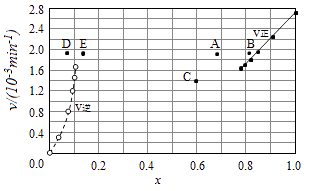
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com