
| A. | CH≡CH+HCl→CH2=CHCl | B. | CH2=CH2+Br2→CH2Br-CH2Br | ||
| C. | 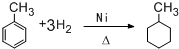 | D. | 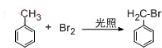 |
分析 有机物中的原子或原子团被其他的原子或原子团所代替生成新的化合物的反应叫取代反应;有机物分子中的不饱和键断裂,断键原子与其他原子或原子团相结合,生成新的化合物的反应是加成反应.
解答 解:A.乙炔中碳碳键断裂和HCl发生加成反应生成氯乙烯,该反应为加成反应,故A错误;
B.乙烯中碳碳双键断裂和溴发生加成反应生成1,2-二溴乙烷,该反应为加成反应,故B错误;
C.苯中大π键发生断裂和氢气发生加成反应生成1-甲基环己烷,该反应为加成反应,故C错误;
D.甲苯中甲基上氢原子被溴原子取代生成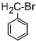 ,该反应为取代反应,故D正确;
,该反应为取代反应,故D正确;
故选D.
点评 本题以反应类型为载体考查有机物结构和性质,为高频考点,明确取代反应和加成反应区别、有机物官能团及其性质关系是解本题关键,能发生加成反应的有烯烃、炔烃、苯环、醛基和羰基等,能发生取代反应的有烷烃、醇、卤代烃、羧酸、酯等,题目难度不大.


科目:高中化学 来源: 题型:解答题
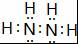 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 利用与氢气的加成反应除去乙烷中的乙烯得到纯净的乙烷 | |
| B. | 利用溴水鉴别苯和甲苯 | |
| C. | 利用酸性高锰酸钾溶液鉴别乙苯和苯乙烯 | |
| D. | 利用四氯化碳萃取溴水中的溴 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 除去乙烷中的少量乙烯:催化剂和加热条件下通入足量的H2 | |
| B. | 除去乙醇中少量的水:加新制生石灰,蒸馏 | |
| C. | 除去溴苯中少量苯:分液 | |
| D. | 除去硝基苯中的HNO3和H2SO4:加入足量NaOH溶液分液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 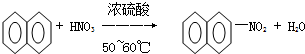 | |
| B. |  | |
| C. | CH3CHO+H2$→_{催化剂}^{高温高压}$CH3CH2OH | |
| D. | 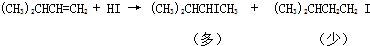 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧化性:F2>C12>Br2 | B. | 酸性:HClO4>H2SO4>H3PO4 | ||
| C. | 熔沸点:SiO2>NaCl>CO2 | D. | 热稳定性:SiH4>PH3>H2S |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ③ | |||||
| 三 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 四 | ⑨ | ⑩ |
 .
. ,该化合物属于离子(填“共价”或“离子”)化合物.
,该化合物属于离子(填“共价”或“离子”)化合物.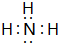 ,该化合物是由极性(填“极性”或“非极性”)键形成的.
,该化合物是由极性(填“极性”或“非极性”)键形成的.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com