


 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案 小学学习好帮手系列答案
小学学习好帮手系列答案科目:高中化学 来源:不详 题型:单选题
| A.X2Y5 | B.XY42- | C.XY2- | D.XY3- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.质子数:a>c>b>d | B.离子的还原性:Y2->Z- |
| C.离子半径:Y2- > Z- > X+ > W3+ | D.元素电负性大小顺序:Y>Z |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.熔点:CO2>KCl>SiO2 | B.水溶性: SO2>HCl>H2S |
| C.还原性:HF>HCl>HBr>HI | D.热稳定性:HF>H2O>NH3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.原子核外电子排布式为1s2的原子与原子核外电子排布式为1s22s2的原子化学性质 相似 |
| B.Fe3+的最外层电子排布式为:3s23p63d5 |
C.基态铜原子的轨道表示式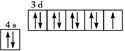 |
D.基态碳原子的轨道表示式 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题


A.Y=2 | B.若X=18,则Z=8 | C.若X=12,它的氧化物化学式为WO | D.若X=15,它属于金属元素的原子 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 较小的是 ;
较小的是 ; 于);
于); 2H2O;②Cl2和H2混合,在光照下就可以发生爆炸,生成HCl。据此推断,活泼性比较:O2 Cl2 (大于/小于);
2H2O;②Cl2和H2混合,在光照下就可以发生爆炸,生成HCl。据此推断,活泼性比较:O2 Cl2 (大于/小于);查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

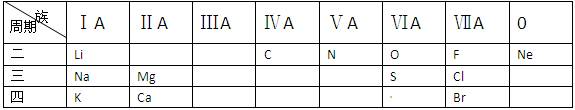
| ① | | | | | | | | | | | | | | | | | |
| | ② | | | | | | | | | | | | ③ | | | | |
| | ④ | | | | | | | | | | | ⑤ | | ⑥ | [ | ⑦ | |
| | ⑧ | | ⑨ | | | | | | | ⑩ | | | | | | | |
 _______________。
_______________。 有一定的相似性,如上表中元素②与元素
有一定的相似性,如上表中元素②与元素 ⑤的氢氧化物有相似的性质。请写出元素②的氢氧化物与NaOH溶液反应的化学方程式:
⑤的氢氧化物有相似的性质。请写出元素②的氢氧化物与NaOH溶液反应的化学方程式:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com