
| △c |
| △t |
| 1mL× 0.01mol/L |
| 1mL+1mL+4mL |
| 1 |
| 6 |
| 1mL× 0.01mol/L |
| 1mL+1mL+4mL |
| 1 |
| 6 |
| ||
| 4s |
| 1 |
| 6 |
| 1 |
| 6 |


 互动课堂系列答案
互动课堂系列答案科目:高中化学 来源: 题型:阅读理解

 +CO2+H2O→
+CO2+H2O→ +NaHCO3
+NaHCO3 +CO2+H2O→
+CO2+H2O→ +NaHCO3
+NaHCO3
|
2- 3 |
2- 6 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解

 +CO2+H2O→
+CO2+H2O→ +NaHCO3;
+NaHCO3; +CO2+H2O→
+CO2+H2O→ +NaHCO3;
+NaHCO3;| 实验操作 | 预期现象 | 现象解释 |
| 步骤1:取少量C放入a试管,加入少量蒸馏水,震荡. | 出现白色浑浊 出现白色浑浊 |
苯酚常温下溶解度不大 苯酚常温下溶解度不大 |
| 步骤2:取少量C的稀溶液分装b、c两只试管,往b试管 滴入过量饱和溴水,振荡. 滴入过量饱和溴水,振荡. |
产生白色沉淀 | 苯酚与溴发生取代反应,生成三溴苯酚白色沉淀. 苯酚与溴发生取代反应,生成三溴苯酚白色沉淀. |
| 步骤3:往c试管 滴入几滴FeCl3溶液,振荡 滴入几滴FeCl3溶液,振荡 |
溶液变为紫色 溶液变为紫色 |
C与加入的试剂发生显色反应. |
| 1 |
| 3 |
| 1 |
| 2 |
| 1000mL |
| 25.00mL |
| 1 |
| 3 |
| 1 |
| 2 |
| 1000mL |
| 25.00mL |
- 3 |
2- 3 |
2- 6 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
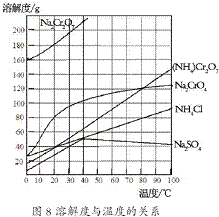 (2012?江苏一模)重铬酸铵[(NH4)2Cr2O7]是一种桔黄色结晶,可用作有机合成催化剂、实验室制纯净的N2及Cr2O3等.实验室可由工业级铬酸钠(Na2CrO4)为原料制取.有关物质溶解度如图所示.实验步骤如下:
(2012?江苏一模)重铬酸铵[(NH4)2Cr2O7]是一种桔黄色结晶,可用作有机合成催化剂、实验室制纯净的N2及Cr2O3等.实验室可由工业级铬酸钠(Na2CrO4)为原料制取.有关物质溶解度如图所示.实验步骤如下:2- 3 |
2- 6 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
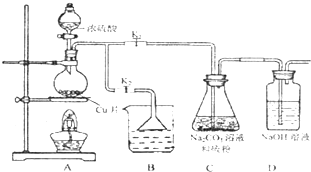 硫代硫酸钠(Na2S2O3)可由亚硫酸钠和硫粉通过化合反应制得.
硫代硫酸钠(Na2S2O3)可由亚硫酸钠和硫粉通过化合反应制得.2- 4 |
2- 7 |
| 编号 | 1 | 2 | 3 | 4 |
| 消耗Na2S2O3标准溶液的体积/mL | 18.02 | 17.98 | 18.00 | 20.03 |
2- 7 |
2- 3 |
2- 6 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com