
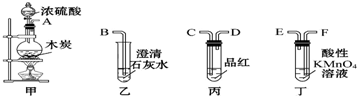
| A. | 按气流从左向右流向,连接装置的正确顺序是A→C→D→F→E→B | |
| B. | 丁中溶液褪色,乙中溶液变浑浊说明甲中生成CO2 | |
| C. | 丙中品红溶液不褪色,乙中溶液变浑浊说明甲中生成CO2 | |
| D. | 丁和丙中溶液都褪色,乙中溶液变浑浊,说明甲中有CO2生成 |
分析 A.根据题中各装置特点及药品可知,甲为气体发生装置、乙为检验二氧化碳装置、丙为检验二氧化硫是否除尽装置、丁为除去二氧化硫的装置,根据实验目的是检验二氧化进行连接装置;
B.若证明有二氧化碳,需要先除去干扰气体二氧化硫,然后使用澄清石灰水检验二氧化碳;
C.若丙中品红不褪色,说明二氧化硫除尽,证明甲中生成了二氧化碳;
D.要证明有二氧化碳生成,必须证明二氧化硫已经除尽,现象为:丁中褪色或颜色变浅,丙中品红不褪色.
解答 解:A.甲为浓硫酸与碳发生反应的装置,高锰酸钾可氧化二氧化硫,用酸性高锰酸钾溶液除SO2,再通过品红溶液不褪色确认SO2已除干净,验证木炭可被浓H2SO4氧化成CO2,可通过二氧化碳能使澄清的石灰水变浑浊确认,所以装置连接顺序为:A→F→E→C→D→B,故A错误;
B.二氧化硫具有漂白性,二氧化硫能使品红褪色,丁装置用高锰酸钾酸性溶液除SO2,再通过品红溶液不褪色,证明二氧化硫已经除尽,若丙中品红褪色,则乙中的澄清的石灰水变浑浊,无法证明甲中反应生成了二氧化碳,故B错误;
C.若丙中品红溶液不褪色,则说明二氧化硫除尽,所以证明甲中有二氧化碳生成,故C正确;
D.丁和丙都褪色,说明二氧化硫没有除尽,二氧化硫影响了二氧化碳的检验,不能根据乙中澄清石灰水不存在判断甲中生成了二氧化碳,故D错误;
故选C.
点评 本题考查了浓硫酸的化学性质、除尽气体的检验方法,题目难度中等,注意掌握浓硫酸与碳、铜等反应的原理,明确检验二氧化硫、二氧化碳混合气体的方法.


 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源: 题型:选择题
| A. | 增加某一反应物的用量一定能够加快该反应的速率 | |
| B. | 化学反应的限度是不可改变的 | |
| C. | 化学反应进行的时间越长该反应的限度越大 | |
| D. | 化学反应达到限度时,正逆反应速率相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | a-n-3 | B. | a+n+3 | C. | a+n-3 | D. | a-n+3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 由于分子间作用力的存在,因而CO2在加热条件下不易发生分解 | |
| B. | 非金属原子间不可能形成离子化合物 | |
| C. | 在PCl3分子中各原子都达到8电子稳定结构 | |
| D. | 离子化合物中可能存在共价键,共价化合物中也可能存在离子键 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 Cu3N的晶胞结构如图,N3-的配位数为6,Cu+半径为acm,N3-半径为bcm,Cu3N的密度为$\frac{103}{4{N}_{A}(a+b)^{3}}$g•cm-3.(阿伏加德罗常数用NA表示,Cu、N相对分子质量为64、14)
Cu3N的晶胞结构如图,N3-的配位数为6,Cu+半径为acm,N3-半径为bcm,Cu3N的密度为$\frac{103}{4{N}_{A}(a+b)^{3}}$g•cm-3.(阿伏加德罗常数用NA表示,Cu、N相对分子质量为64、14)查看答案和解析>>
科目:高中化学 来源: 题型:解答题
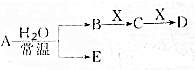 已知A、B、C、D、E、X的转化关系如图所示:
已知A、B、C、D、E、X的转化关系如图所示:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com