
 MgCu2+3MgH2
MgCu2+3MgH2

科目:高中化学 来源:不详 题型:单选题
A.对硝基甲苯的结构简式: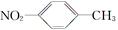 |
B.CH2F2的电子式: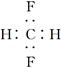 |
| C.16O2与18O2互为同素异形体 |
| D.乙炔的最简式:CH |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
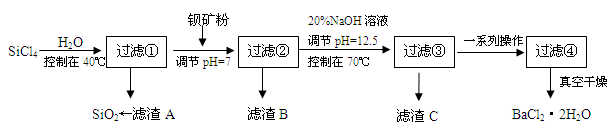
 溶液和
溶液和 溶液(中性)。请结合平衡原理和必要的文字解释滤渣C能溶于3mol/L的
溶液(中性)。请结合平衡原理和必要的文字解释滤渣C能溶于3mol/L的 溶液的原因______。
溶液的原因______。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
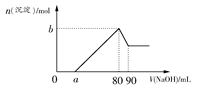
| A.盐酸的体积为80 mL |
| B.a的取值范围为0<a<50 |
| C.n(Mg2+)<0.025 mol |
| D.当a值为30时,b值为0.01 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.H2S和SO2 | B.NO和O2 | C.NH3和HCl | D.Cl2和H2S |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.标准状况下,22.4 L苯中含有的分子数目为NA |
| B.25℃、101 kPa时,20 g SO3中含有的原子数目为NA |
| C.1 L 1 mol·L-1 MgCl2溶液中含有的氯离子数目为NA |
| D.16.8 g Fe与足量水蒸气反应,转移的电子数目为0.9NA |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.含有金属元素的离子一定是阳离子,金属阳离子被还原一定得到金属单质 |
| B.pH相等的NaOH、NaHCO3和Na2CO3三种溶液: c(NaOH)<c(NaHCO3)<c(Na2CO3) |
| C.常温下,c(NH4+)相等的4种溶液:①(NH4)2SO4②(NH4)2Fe(SO4)2③NH4Cl ④(NH4)2CO3,溶质物质的量浓度大小关系是:②<①<④<③ |
| D.某温度时水的离子积常数KW=10-13若将此温度下pH=11的NaOH溶液aL与pH=1的稀硫酸bL混合,若所得混合液pH=2,则a:b=2:9 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 Ag2O2↓+2KNO3+2K2SO4+2H2O
Ag2O2↓+2KNO3+2K2SO4+2H2O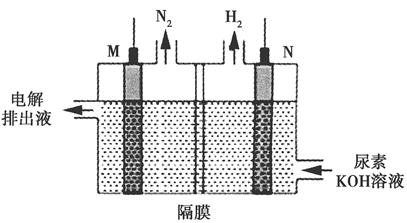
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.中子数为14的硅原子: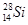 |
B.CH4分子的比例模型: |
C.聚乙烯的结构简式: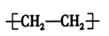 |
| D.次氯酸分子的结构式:H—O-Cl |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com