
 Ag2O2↓+2KNO3+2K2SO4+2H2O
Ag2O2↓+2KNO3+2K2SO4+2H2O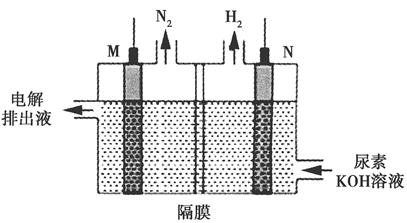


 期末集结号系列答案
期末集结号系列答案科目:高中化学 来源:不详 题型:单选题
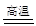 2Fe + Al2O3,下列说法中正确的是( )
2Fe + Al2O3,下列说法中正确的是( )| A.Fe元素的化合价升高 | B.若27 g Al参加反应则有3 mol电子转移 |
| C.Fe2O3发生氧化反应 | D.Al被还原 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
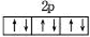

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.失电子越多,该物质的还原性就越强 |
| B.含有最高价元素的化合物一定具有强氧化性 |
| C.氧化剂氧化其他物质时,本身被还原 |
| D.某元素由化合态变成游离态一定被还原 |
查看答案和解析>>
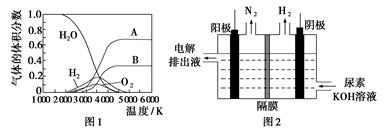
科目:高中化学 来源:不详 题型:单选题
| A.废水处理时铝单质转化为Al3+ | B.废水处理中,亚硝酸盐被还原 |
| C.处理过程中,OH一参与了反应 | D.铝粉颗粒大小影响废水处理的速率 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
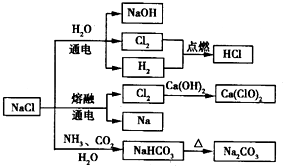
| A.25℃,NaHCO3在水中的溶解度比Na2CO3的大 |
| B.石灰乳与Cl2的反应中,Cl2既是氧化剂,又是还原剂 |
| C.常温下干燥的Cl2能用钢瓶贮存,所以Cl2不与铁反应 |
| D.图中所示转化反应都是氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.标准状况下,11.2L的己烷所含的分子数为0.5NA个 |
| B.28g乙烯所含共用电子对数目为4NA个 |
| C.标准状况下,11.2 L二氯甲烷所含分子数为0.5 NA个 |
| D.现有乙烯、丙烯、丁烯的混合气体共14g,其原子数为3NA个 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.H2O2、Na2O2都属于过氧化物,都存在共价键 |
| B.双氧水是绿色氧化剂,可作医疗消毒剂 |
| C.H2O2既有氧化性,又有还原性,与Cl2、KMnO4反应是表现H2O2的氧化性 |
| D.H2O2做漂白剂是利用其氧化性,漂白原理与HClO类似,与SO2不同 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com