


科目:高中化学 来源: 题型:
| A、氢氧化钠溶液与醋酸溶液反应的离子方程式为:H++OH-═H2O |
| B、相同物质的量浓度盐酸与氨水溶液等体积混合后c(CI-)>c(NH4+)>c(OH-)>c(H+) |
| C、常温下,由水电离出的c(H+)=1×10-12mol/L的溶液中,Fe2+、NO3-、Na+、SO42-一定能大量共存 |
| D、硫酸铝溶液蒸干后得到硫酸铝固体,氯化铁溶液蒸干后得到氢氧化铁固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、人工合成药物只有阿司匹林 |
| B、1853年,德国拜尔药厂的化学家霍夫曼合成了乙酰水杨酸 |
| C、青霉素是人工合成药物中的其中一种 |
| D、抗酸药除了含有碳酸氢钠、氢氧化铝和盐酸物质外,还含有调味剂和黏合剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
 向含Fe2+、I-、Br-的溶液中通入过量的氯气.溶液中四种粒子的物质的量变化如图所示.已知b-a=5;线段IV表示一种含氧酸,且I和IV表示的物质中含有相同的元素.
向含Fe2+、I-、Br-的溶液中通入过量的氯气.溶液中四种粒子的物质的量变化如图所示.已知b-a=5;线段IV表示一种含氧酸,且I和IV表示的物质中含有相同的元素.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
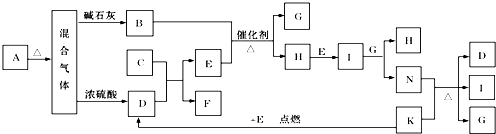
查看答案和解析>>
科目:高中化学 来源: 题型:
| 2SO2(g)+O2?2SO3(g) | 大气 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com