
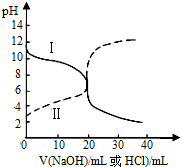
 25℃时,取浓度均为0.1mol•L-1的醋酸溶液和氨水溶液各20mL,分别用0.1mol•L-1NaOH溶液、0.1mol•L-1盐酸进行中和滴定,滴定过程中pH随滴加溶液的体积变化关系如图所示.下列说法正确的是( )
25℃时,取浓度均为0.1mol•L-1的醋酸溶液和氨水溶液各20mL,分别用0.1mol•L-1NaOH溶液、0.1mol•L-1盐酸进行中和滴定,滴定过程中pH随滴加溶液的体积变化关系如图所示.下列说法正确的是( )| A. | 曲线Ⅰ:滴加溶液到10 mL时:c(NH4+)>c(NH3•H2O)>c(Cl-)>c(OH-)>c(H+) | |
| B. | 曲线Ⅱ:滴加溶液到20 mL时:2c(CH3COO-)+c(CH3COOH)+c(OH-)═2c(Na+)+c(H+) | |
| C. | 根据滴定曲线,可得Kb(NH3•H2O)≈10-13 | |
| D. | 由曲线Ⅱ可知,选用酚酞和选用甲基橙作指示剂,消耗NaOH溶液的体积相同 |
分析 根据曲线变化趋势知,当未滴加溶液时,曲线I的pH>7,说明属于酸滴定碱溶液,根据曲线变化趋势知,当未滴加溶液时,曲线II的pH<7,说明属于碱滴定酸溶液;
A.曲线I是用盐酸滴定氨水,滴加溶液到10mL时,得到等物质的量的NH4Cl和一水合氨,溶液呈碱性;
B.曲线Ⅱ是用氢氧化钠滴定醋酸,滴加溶液到20mL时,得到的是醋酸钠,根据电荷守恒、物料守恒解答;
C.根据图象可知,0.1000mol/L的氨水的pH约为11,据此计算出Kb(NH3•H2O);
D.甲基橙的变色范围就是3.1-4.4,酚酞的是8.2-10.
解答 解:根据曲线变化趋势知,当未滴加溶液时,曲线I的pH>7,说明属于酸滴定碱溶液,根据曲线变化趋势知,当未滴加溶液时,曲线II的pH<7,说明属于碱滴定酸溶液;
A.曲线I是用盐酸滴定氨水,滴加溶液到10mL时,得到等物质的量的NH4Cl和一水合氨,溶液呈碱性,说明氨水的电离程度大于NH4Cl的水解,则c(Cl-)>c(NH4+)>c(NH3•H2O)>c(OH-)>c(H+),故A错误;
B.曲线Ⅱ是用氢氧化钠滴定醋酸,滴加溶液到20mL时,得到的是醋酸钠,由物料守恒知:c(CH3COOH)+c(CH3COO-)=c(Na+),由电荷守恒知:c(OH-)+c(CH3COO-)=c(Na+)+c(H+),两式相加即得:2c(CH3COO-)+c(CH3COOH)+c(OH-)═2c(Na+)+c(H+),故B正确;
C.结合图象可知,0.1000mol/L的氨水的pH约为11,c(OH-)=c(NH4+)=0.001mol/L,Kb(NH3•H2O)=$\frac{c(O{H}^{-})•c(N{{H}_{4}}^{+})}{c(N{H}_{3}•{H}_{2}O)}$=$\frac{1{0}^{-3}×1{0}^{-3}}{0.1}$≈10-5,故C错误;
D.曲线Ⅱ是用氢氧化钠滴定醋酸,甲基橙的变色范围就是3.1-4.4,酚酞的是8.2-10,使酚酞变色要碱性,需多消耗些NaOH溶液,故D错误;
故选B.
点评 本题考查了酸碱混合溶液定性判断,根据溶液中的溶质及其性质结合电荷守恒和物料守恒来分析解答,题目难度中等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
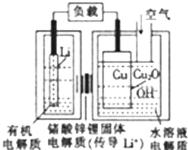 某锂电池的结构如图所示,该电池放电过程中的一个电极反应式为Cu2O+2e-+H2O=2Cu+2OH-,下列说法正确的是( )
某锂电池的结构如图所示,该电池放电过程中的一个电极反应式为Cu2O+2e-+H2O=2Cu+2OH-,下列说法正确的是( )| A. | 放电时,Li+透过固体电解质向Li极移动 | |
| B. | 放电时,负极的电极反应式为Li-e-+OH-=LiOH | |
| C. | 放电时,水溶液的pH不断升高 | |
| D. | 放电过程中需要不断地补充Cu |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 基于硫代硫酸钠与稀硫酸反应生成S和SO2,在定量测定反应速率时,既可用S对标记遮盖法,也可用排水法测SO2体积,计算出其反应速率 | |
| B. | 将两块未擦去氧化膜的铝片分别投入1mol?L-1CuSO4溶液、1mol?L-1CuCl2溶液中,一段时间后,铝片表面都观察不到明显的反应现象 | |
| C. | 将20g硝酸钠和17g氯化钾放入100ml烧杯中,加35mL水,并加热、搅拌,使溶液浓缩至约为原来的一半时,趁热过滤即可得到硝酸钾晶体 | |
| D. | 试管内壁附着的硫黄可以用热的KOH溶液洗涤,也可以用CS2洗涤 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将铜片放入浓硫酸中,无明显实验现象,说明铜在冷的浓硫酸中发生钝化 | |
| B. | 油脂制肥皂实验中加乙醇的目的是增大油脂的溶解度从而加快油脂皂化反应速率 | |
| C. | 工业合成氨的反应属于能自发进行的反应,故能迅速发生 | |
| D. | 鸡蛋清溶液中加入饱和Na2SO4溶液有沉淀生成是因为蛋白质变性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
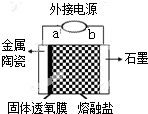 我国科学家最新研发的固体透氧膜提取金属钛工艺,其电解装置如图所示:将TiO2熔于NaCl-NaF融盐体系,以石墨为阴极,覆盖氧渗透膜的多孔金属陶瓷涂层为阳极,固体透氧膜把阳极和熔融电解质隔开,只有O2-可以通过.下列说法不正确的是( )
我国科学家最新研发的固体透氧膜提取金属钛工艺,其电解装置如图所示:将TiO2熔于NaCl-NaF融盐体系,以石墨为阴极,覆盖氧渗透膜的多孔金属陶瓷涂层为阳极,固体透氧膜把阳极和熔融电解质隔开,只有O2-可以通过.下列说法不正确的是( )| A. | a 极是电源的正极,Ti4+在熔融盐中从左往右迁移 | |
| B. | 阳极电极反应式为2Cl--2e-=Cl2↑ | |
| C. | 已知每摩尔电子的电量为965 00 C,理论上生成48mg钛,则电解过程中通过电解池的电量为386 C | |
| D. | NaCl-NaF融盐的作用是降低熔化TiO2需要的温度 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
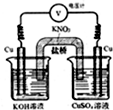 实验室利用如图所示装置.通过测电压求算Cu(OH)2的沉淀溶解平衡常数,工作一段时间后,两电极质量均增大.下列说法不正确的是( )
实验室利用如图所示装置.通过测电压求算Cu(OH)2的沉淀溶解平衡常数,工作一段时间后,两电极质量均增大.下列说法不正确的是( )| A. | 该装置工作时化学能转化为电能 | B. | 左池中的铜电极作正极 | ||
| C. | 总反应为Cu2+(aq)+2OH-(aq)?Cu(OH)2(s) | D. | 盐桥中的K+移向CuSO4溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
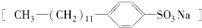 是常用洗涤剂的主要成分.其结构可用图形
是常用洗涤剂的主要成分.其结构可用图形 来表示,•端为链烃基,O端为极性基.根据这一结构特点,试分析和回答下列问题:
来表示,•端为链烃基,O端为极性基.根据这一结构特点,试分析和回答下列问题: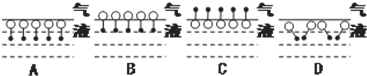
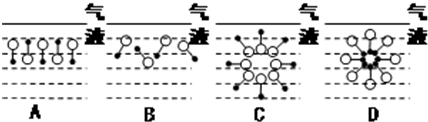
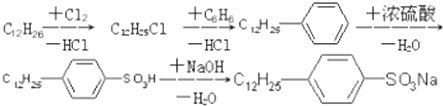
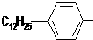 .
.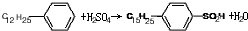 ,反应类型为取代反应.
,反应类型为取代反应.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com