
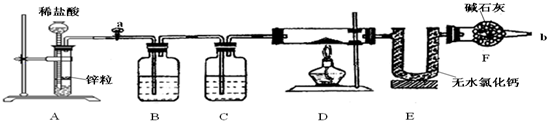
分析 装置A是制备氢气的发生装置,通过装置B中的水除去氢气中的氯化氢,通过装置C中的浓硫酸干燥氢气,通过装置D还原FeO和Fe2O3的混合物,生成的水蒸气进入装置E吸收,称量质量变化得到生成水的质量计算氧化铁的质量,装置F是防止空气中的水蒸气进入装置E影响测定结果的准确性,
(1)氢气是可燃性气体加热或点燃前需要进行验纯;
(2)A中产生的H2中混有HCl和水蒸气,必须通过洗气逐一除去,防止干扰后续实验;
(3)可用浓硫酸干燥氢气;
(4)若无干燥管F,空气中的水蒸气被E吸收则所测生成水的质量增大,氧元素物质的量偏大.
解答 解:(1)氢气是可燃性气体,装置中需要充满氢气后方可进行加热反应,所以需要对氢气进行验纯,避免混有空气加热发生爆炸,在F处b口收集氢气验纯;
故答案为:检验氢气的纯度;
(2)由于A中产生的H2中混有HCl和水蒸气,必须通过洗气逐一除去,防止干扰后续实验,所以B的作用是除去氢气中的氯化氢,
故答案为:出去氢气中混有的HCl气体;
(3)C中为浓硫酸,用于干燥氢气,故答案为:浓硫酸;
(4)干燥管F的作用防空气中水蒸气对实验干扰,若无干燥管F,空气中的水蒸气被E吸收则所测生成水的质量增大,导致氧的含量增大,Fe2O3的质量将偏大,
故答案为:偏大.
点评 本题考查了测定FeO和Fe2O3固体混合物中Fe2O3的质量,是一道综合实验题,解题的关键是掌握各种装置的作用,并能根据相关的数据进行计算,此题对训练学生思维能力有一定帮助,本题难度中等


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
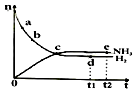 合成氨工业对国民经济和社会发展具有重要的意义.对于密闭容器中的反应:
合成氨工业对国民经济和社会发展具有重要的意义.对于密闭容器中的反应:| A. | 点d(t1时刻)和点e(t2时刻)处n(N2)不一样 | |
| B. | 点c处反应达到平衡 | |
| C. | 点a的正反应速率比点b的大 | |
| D. | 其他条件不变,773 K下反应至t1时刻,n(H2)比图中d点的值小 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
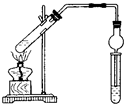 用图所示实验装置制取乙酸乙酯.回答以下问题:
用图所示实验装置制取乙酸乙酯.回答以下问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
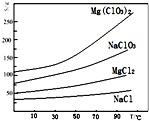 氯酸镁[Mg(ClO3)2]常用作催熟剂、除草剂等,实验室用卤块(主要成分为MgCl2•6H2O,含有MgSO4、FeCl2等杂质)制备少量Mg(ClO3)2•6H2O的流程如下:
氯酸镁[Mg(ClO3)2]常用作催熟剂、除草剂等,实验室用卤块(主要成分为MgCl2•6H2O,含有MgSO4、FeCl2等杂质)制备少量Mg(ClO3)2•6H2O的流程如下:查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 对于同一个化学反应,一步完成和分几步完成,其反应的焓变不相同 | |
| B. | 如果某化学反应的△H和△S均小于0,则反应一定能自发进行 | |
| C. | 化学反应过程中,断键吸热,成键放热 | |
| D. | 反应物的总焓大于反应产物的总焓时,△H>0 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向次氯酸钙溶液通入过量CO2:Ca2++2ClO-+H2O+CO2═CaCO3↓+2HClO | |
| B. | 向Ca(HCO3)2溶液中加入少量的NaOH溶液:Ca2++2HCO3-+2OH-═CaCO3↓+CO32-+H2O | |
| C. | 硫代硫酸钠溶液中加入硫酸:S2O32-+6H++2SO42-═4SO2↑+3H2O | |
| D. | 酸性溶液中KIO3与KI反应生成I2:IO3-+5I-+6H+═3I2+3H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com