
【题目】采用电化学方法以SO2和Na2SO3为原料制取硫酸的装置如图所示(A、B为多孔石墨电极,C、D为惰性电极)。下列说法错误的是( )

A.“膜2”为阳离子交换膜
B.电极A的电极反应为SO2-2e-+2H2O==SO42-+4H+
C.上述过程中,亚硫酸钠溶液可循环使用
D.使用该装置制取98g硫酸需消耗11.2L O2(STP)
【答案】D
【解析】
根据装置图,生成氢气的一极为阴极,所以电极D为阴极,得到电子,发生还原反应,其电极反应为:2HSO3-+2e-=2SO32-+H2↑,电极C为阳极,失去电子,发生氧化反应,其电极反应式为:HSO3--2e-+H2O =SO42-+3H+;电极A为负极,二氧化硫失去电子生成硫酸根离子,发生氧化反应,其电极反应式为:SO2-2e-+2H2O==SO42-+4H+;电极B为正极,氧气得到电子,发生还原反应,其电极反应式为:O2+4e-+4H+=2H2O。
A. 电极D为阴极,溶液中的阳离子移向阴极,所以“膜2”为阳离子交换膜,A正确;
B. 电极A为负极,二氧化硫失去电子生成硫酸根离子,发生氧化反应,其电极反应为:SO2-2e-+2H2O=SO42-+4H+,B正确;
C. 根据装置图,X为Na2SO3,与SO2反应,生成NaHSO3,NaHSO3到溶液中又生成Na2SO3,所以Na2SO3溶液可循环使用,C正确;
D. 左侧室的总反应为:2SO2+ O2+2H2O=2H2SO4,右侧室的总反应为3HSO3-+ H2O=2SO32-+H2↑+SO42-+3H+,制取98g硫酸,标准状况下消耗不了11.2L O2,D错误;故答案为:D。


科目:高中化学 来源: 题型:
【题目】碳酸盐燃料电池,以一定比例的Li2CO3和Na2CO3低熔混合物为电解质,操作温度为650℃,在此温度下以镍为催化剂,以煤气(CO、H2的体积比为3:1)直接作燃料,其工作原理如图所示,并以此电源用于工业生产。
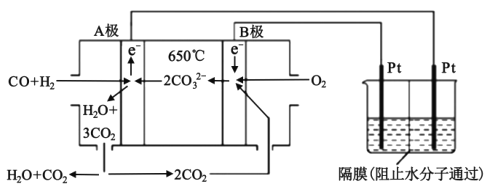
(1)H2(g)、CO(g)的燃烧热△H分别为-285.8kJmol-1、-283.0kJmol-1,18g液态水变为水蒸气时吸热44.0kJ,则电池总反应3CO(g)+H2(g)+2O2(g)=3CO2(g)+H2O(g)的△H=___kJmol-1,B电极上发生反应的电极反应式为___。
(2)若以此电源生产新型硝化剂N2O5,装置如图所示。已知两室加入的试剂分别是a.硝酸溶液;b.N2O4+无水硝酸,则左室加入的试剂应为___(填“a”或“b”),其电极反应式为___。
(3)若以此电源用惰性电极电解足量的硝酸银溶液,阴极产物的质量为5.4g,则阳极产生的气体在标准状况下的体积为___L。电解后溶液体积为500mL,溶液的pH约为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知化学反应A2(g)+B2(g)=2AB(s)的能量变化如图所示,下列叙述正确的是

A. 该反应为放热反应
B. A—B的键能为bkJmol-1
C. 加催化剂能降低该反应焓变
D. 该反应的反应热为△H=(a-b)kJmol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】到目前为止,由化学能转变的热能或电能仍然是人类使用的最主要的能源.
(1)在25℃、101kPa下,16g的甲醇(CH3OH)完全燃烧生成CO2和液态水时放出352kJ的热量,则表示甲醇燃烧热的热化学方程式为_____________________。
(2)化学反应中放出的热能(焓变,△H)与反应物和生成物的键能(E)有关.
已知:H2(g)+Cl2(g)=2HCl(g)△H=﹣185kJ/mol,
E(H﹣H)=436kJ/mol,E(Cl﹣Cl)=243kJ/mol则E(H﹣Cl)=_____________
(3)纳米级Cu2O由于具有优良的催化性能而受到关注.已知:
2Cu(s)+![]() O2(g)═Cu2O(s)△H=﹣169kJmol﹣1,
O2(g)═Cu2O(s)△H=﹣169kJmol﹣1,
C(s)+![]() O2(g)═CO(g)△H=﹣110.5kJmol﹣1,
O2(g)═CO(g)△H=﹣110.5kJmol﹣1,
2Cu(s)+O2(g)═2CuO(s)△H=﹣314kJmol﹣1
则工业上用炭粉在高温条件下还原CuO制取Cu2O和CO的热化学方程式_____________。
(4)如图是N2和H2反应生成2molNH3过程中能量变化示意图:

①请计算每生成1molNH3放出热量为:_________.
②若起始时向容器内放入1molN2和3molH2达平衡后N2的为20%,则反应放出的热量为Q1kJ,则Q1的数值为_________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某种氨硼烷(NH3·BH3)电池装置如图所示(未加入氨硼烷之前,两极室内液体质量相等),电池反应为NH3·BH3+3H2O=NH4BO2+4H2O(不考虑其他反应的影响)。下列说法错误的是( )
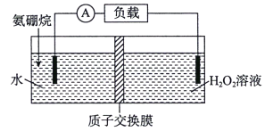
A.氨硼烷中N和B的杂化方式不同
B.电池正极的电极反应式为H2O2+2H++2e-=2H2O
C.其他条件不变,向H2O2溶液中加入适量硫酸能增大电流强度
D.若加入的氨硼烷全部放电后左右两极室内液体质量差为3.8g,则电路中转移1.2mol电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表中的各组物质之间通过一步反应就能实现如图所示转化的是( )
编号 | a | b | c | d |
|
① | Na2O | Na2O2 | Na | NaOH | |
② | Al2O3 | NaAlO2 | Al | Al(OH)3 | |
③ | FeCl2 | FeCl3 | Fe | CuCl2 | |
④ | MgO | MgCl2 | Mg | Mg(OH)2 |
A.①②④B.①③④C.①②③D.②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,反应N2 + 3H2![]() 2NH3,在2L密闭容器中进行,5min内氨的质量增加了1.7 g,则反应速率为
2NH3,在2L密闭容器中进行,5min内氨的质量增加了1.7 g,则反应速率为
A.v(H2)=0.03 mol/(L·min)B.v(N2)=0.02mol/(L·min)
C.v(NH3)=0.01mol/(L·min)D.v(NH3)=0.17mol/(L·min)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图表示800℃时A、B、C三种气体的物质的量浓度随时间变化的情况,t时各组分浓度不再变化。试回答:

(1)该反应的反应物是_____,达平衡时其转化率是___。
(2)该反应的化学方程式是______。
(3)若t是2min,A物质的平均反应速率是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温时,向120 mL 0.005 mol·L-1 CaCl2溶液中逐滴加入0.1 mol·L-1 Na2CO3溶液,混合溶液的电导率变化曲线如图所示。已知25℃时,Ksp(CaCO3)=3.36×10-9,忽略CO32-水解。下列说法正确的是
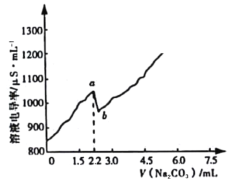
A.a点对应的溶液中Ca2+开始形成沉淀,溶液中c(Ca2+)=c(CO32-)
B.b点对应的溶液中Ca2+已完全沉淀,且存在关系:c(Na+)+c(H+)=c(Cl-)+c(OH-)
C.在滴加Na2CO3溶液的过程中,混合溶液的pH先减小后增大
D.右图可以说明CaCO3在溶液中存在过饱和现象
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com