
【题目】三室式电渗析法处理含Na2SO4废水的原理如图所示,采用惰性电极,ab、cd均为离子交换膜,在直流电场的作用下,两膜中间的Na+和S![]() 可通过离子交换膜,而两端隔室中离子被阻挡不能进入中间隔室。下列叙述正确的是 ( )
可通过离子交换膜,而两端隔室中离子被阻挡不能进入中间隔室。下列叙述正确的是 ( )
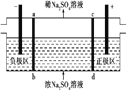
A. 通电后中间隔室的S![]() 离子向正极迁移,正极区溶液pH增大
离子向正极迁移,正极区溶液pH增大
B. 当电路中通过1 mol电子的电量时,会有0.5 mol的O2生成
C. 负极反应为2H2O-4e-![]() O2+4H+,负极区溶液pH降低
O2+4H+,负极区溶液pH降低
D. 该法在处理含Na2SO4废水时可以得到NaOH和H2SO4产品
科目:高中化学 来源: 题型:
【题目】下列表示对应化学反应的离子方程式正确的是
A. FeCl3溶液与Cu的反应:Cu+Fe3+==Cu2++Fe2+
B. NO2与水的反应:3NO2+H2O==2NO3-+NO+2H+
C. 醋酸溶液与水垢中的CaCO3反应:CaCO3+2H+==Ca2++H2O+CO2![]()
D. 向NaAlO2溶液中通入过量CO2:2AlO2-+CO2+3H2O==2Al(OH)3![]() +CO32-
+CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机物的叙述正确的是
A. 分子式相同而结构不同的化合物互称为同分异构体
B. 凡是分子组成相差一个或几个CH2原子团的物质,彼此一定是同系物
C. 两种化合物组成元素相同,各元素质量分数也相同,则两者一定是同种物质
D. 羧基、醛基、羟基、乙基都属于有机物的官能团
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知硼、氮、钴、铜是几种重要的元素,请回答下列向题:
(1)Co的基态原子中未成对电子数为________个;Cu的基态原子的电子排布式为_______。
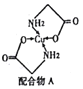
(2)Cu的配合物A的结构如右图,A中所含C、N、O三种元素的第一电离能由大到小的顺序为________。其中氮原子的杂化方式是_______________。
(3)配体氨基乙酸根(H2NCH2COO-)受热分解可产生CO2 和N2, N2中δ键和π键数目之比是________;N2O与CO2互为等电子体,结构相似,且N2O分子中O只与一个N相连,则N2O的电子式为________。
(4)立方氮化硼的晶胞结构与金刚石结构相似(如下图),是超硬材料。

①晶胞中每个氮原子周围与其最近且等距离的硼原子有________个;
②结构化学上常用原子坐标参数表示晶胞内部各原子的相对位置,立方氮化翻的晶胞中,B原子的坐标参数分别有:B (0,0,0);B(![]() ,0,
,0, ![]() );B (
);B (![]() ,(
,(![]() ,
, ![]() ,0)等,则距离上述三个B原子最近且等距离的N原子的坐标参数为_________;
,0)等,则距离上述三个B原子最近且等距离的N原子的坐标参数为_________;
③已知氮化硼晶胞边长为apm,则氮化硼的密度为_______g·cm -3(设NA为阿伏加德罗常数值,只要求列算式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质能按照如图关系图(“→”表示反应一步完成)相互转化的是

A | B | C | D | |
X | NaOH | Cu | Fe2O3 | Ca(OH)2 |
Y | NaNO3 | CuO | Fe | CaCl2 |
Z | Na2SO4 | Cu(OH)2 | FeCl2 | CaCO3 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
已知化合物Z(4 -乙酰氨基苯甲酸乙酯)是重要的化工中间体,其一种合成路径如下:
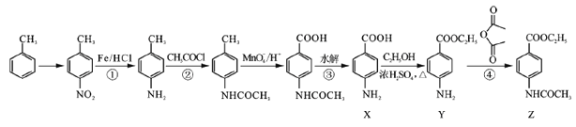
(1)反应①的反应类型为____________,Y中的含氧官能团名称为____________。
(2)合成路径中反应②、③的目的是_________________。
(3)试剂X可以脱水缩合为一种链状高分子化合物,其结构简式为__________________。
(4)写出反应④的化学方程式_____________________。
(5)Y是一种医用麻醉剂,其符合下列条件的同分异构体数目为________________种。
①苯环上有两个取代基,其中一个为氨基(—NH2)且与苯环直接相连;
②能发生水解反应。
写出其中能发生银镜反应且核磁共振氢谱中峰最少的同分异构体的结构简式_________________。
(6)某同学进一步优化了上述合成路线,发现经三步反应即可将![]() 转化成
转化成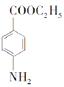 ,请写出该同学的合成路线(无机试剂任选)。________
,请写出该同学的合成路线(无机试剂任选)。________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】欧洲、美国、日本已构成世界上最先进的香料香精工业中心,并且以香精为龙头产品带动天然香料和合成香料的发展。我国食用香精香料行业呈现外资企业和民营企业两强争霸的剧烈竞争态势。某芳香化合物的结构简式如图:该物质的苯环上的n溴代物的同分异构体的数目和m溴代物的同分异构体的数目相等,则n和m一定满足的关系式是 ( )
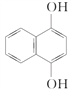
A. n+m=8 B. n+m=7 C. 2n=m D. n+m=6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镁及其合金是一种用途很广的金属材料,目前世界上60%的镁是从海水中提取出来的。主要步骤如下:

(1)为了使MgSO4转化为Mg(OH)2,试剂①可以选用__________,要使MgSO4完全转化为沉淀,加入试剂①的量应________。
(2)加入试剂①后,能够分离得到Mg(OH)2沉淀的方法是_____________。
(3)试剂②可以选用____________。
(4)无水MgCl2在熔融状态下电解,会生成Mg和Cl2,写出该反应的化学方程式:__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】粗盐中往往含有Ca2+、Mg2+、SO42-,为了有效除去该杂质离子,加入试剂的合理顺序为( )
A. 先加NaOH,后加Na2CO3,再加BaCl2
B. 先加NaOH,后加BaCl2,再加Na2CO3
C. 先加Na2CO3,后加NaOH,再加BaCl2
D. 先加Na2CO3,后加BaCl2,再加NaOH
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com