
下列离子方程式正确的是
| A.向CuSO4溶液中投入Na:Cu2++2Na=Cu+2Na+ |
| B.向FeCl3溶液中滴加KSCN溶液:Fe3++3SCN-=Fe(SCN)3↓ |
| C.向NaHCO3溶液中加过量Ca(OH)2溶液:Ca2++HCO3-+OH-=CaCO3↓+H2O |
| D.向BaCO3固体中加入过量的稀H2SO4:BaCO3+2H+=Ba2++CO2↑+H2O |
C
解析试题分析:硫酸铜溶液是盐溶液,钠与水反应比钠与硫酸铜反应容易得多、剧烈得多,即2Na+2H2O=2Na++2OH-+H2↑,2OH-+Cu2+=Cu(OH)2↓,总反应式为2Na+2H2O+Cu2+=Cu(OH)2↓+2Na++H2↑,故A错;氯化铁溶液与硫氰化钾溶液发生显色反应,得到红色的硫氰化铁溶液和氯化钾,因此硫氰化钾不能标沉淀符号,故B错;设碳酸氢钠的系数为1,则与过量氢氧化钙溶液的反应为NaHCO3+Ca(OH)2=CaCO3↓+NaOH+H2O,则离子方程式为Ca2++HCO3-+OH-=CaCO3↓+H2O,故C正确;钡离子与硫酸根离子反应,生成硫酸钡沉淀,因此反应后无钡离子存在,碳酸钡难溶于水,但硫酸的酸性比碳酸强,则碳酸钡与过量的硫酸完全反应,生成硫酸钡、二氧化碳气体和水,BaCO3+2H++SO42-=BaSO4+CO2↑+H2O,故D错。
考点:考查离子方程式,涉及金属钠与硫酸铜溶液反应的先后、氯化铁溶液与硫氰化钾溶液的反应、碳酸氢钠与过量氢氧化钙溶液的反应、碳酸钡与过量硫酸反应等。


科目:高中化学 来源: 题型:单选题
某无色溶液M可能含有离子OH-、HCO3-、CO32-、SO42-、SiO32-、AlO2-、NH4+、MnO4-、Cu2+、Mg2+、Na+、Fe3+中的若干种。取一定量的M溶液滴加盐酸,产生沉淀的物质的量与盐酸体积的关系如图所示。下列判断正确的是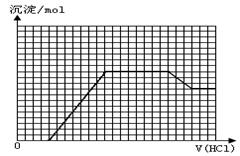
| A.原溶液中可能含有NH4+、SO42- |
| B.最终溶液中最少含2种溶质 |
| C.原溶液中n(NaAlO2):n(Na2CO3)=1:1 |
| D.滴加盐酸初始阶段发生反应的离子方程式是:CO32-+H+=HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
在水溶液中能大量共存的一组是
| A.Ba2+、Na+、SO42-、Cl- | B.MnO4-、SO32-、H+、K+ |
| C.AlO2-、Mg2+、K+、HCO3- | D.K+、Na+、NO3-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
在溶液中能大量共存的一组离子或分子是
| A.K+、Al3+、SO42―、NH3·H2O | B.NH4+、H+、NO3―、HCO3― |
C.Na+、CH3COO―、CO32―、OH― | D.Na+、K+、SO32―、Cl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
在水溶液中能大量共存的一组离子是
| A.H+、K+、Cl-、CO32- | B.Ba2+、Na+、SO42-、Cl- |
| C.ClO-、I-、K+、Mg2+ | D.Mg2+、K+、SO42-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
能在水溶液中大量共存的一组离子是
| A.H+、Fe3+、I-、SO42- |
| B.Al3+、Mg2+、HCO3-、Cl- |
| C.K+、Ca2+、NO3-、SiO32- |
| D.K+、Na+、OH-、AlO2- |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列离子组在溶液中能大量共存的是
| A.Fe3+、SCN-、I-、K+ |
| B.K+、Al3+、SO42-、MnO4- |
| C.H+、NO3-、Fe2+、Na+ |
| D.Cu2+、NH4+、Br-、OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
在下列溶液中,各组离子一定能够大量共存的是
| A.pH=2的溶液:Fe3+、Cu2+、SO42-、NO3- |
| B.c(H+)=1×10-12mol/L的溶液:NH4+、K+、Cl-、AlO2- |
| C.水电离的c(H+)=1×10-12mol/L的溶液:Na+、Al3+、Br-、ClO- |
| D.与铝反应放出氢气的溶液:Na+、Mg2+、Br-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(10分)已知反应:3NO2+H2O==2HNO3+NO,回答下列问题:
(1)该反应的离子方程式为 。
(2)氧化剂与还原剂的质量比为 ,氧化产物与还原产物的物质的量之比为 。
(3)在标准状况下,3.36L NO2与H2O完全反应转移的电子数目为 。
(4)写出HNO3与石灰水反应的离子方程式 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com