
| A、300mL 1mol/L的硝酸钠溶液 |
| B、200mL 1.5mol/L的硝酸镁溶液 |
| C、100mL 1.5mol/L的硝酸铝溶液 |
| D、200mL 3mol/L的硝酸钾溶液 |


科目:高中化学 来源: 题型:
| A、③ | B、②③ | C、①② | D、①②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氧化性由强到弱顺序是:KMnO4>Cl2>Fe3+>I2 |
| B、还原性由强到弱顺序是:Mn2+>Cl->Fe2+>I- |
| C、I--与Fe3+能在溶液中发生氧化还原反应 |
| D、在溶液中可以发生2KCl+I2=Cl2+2KI反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Z为0.3 mol/L |
| B、Y为0.15 mol/L |
| C、X为0.1 mol/L |
| D、Z为0.35mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温下,SiO2性质较稳定,不与所有的酸发生反应 |
| B、硅酸钠的水溶液俗称水玻璃,可作防火材料 |
| C、硅是一种亲氧元素,在地壳中的含量仅次于氧 |
| D、玻璃、陶瓷、水泥都属于硅酸盐产品 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、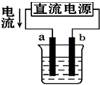 用装置精炼铜,则a极为粗铜,电解质溶液为CuSO4溶液 |
B、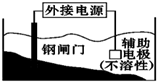 装置中钢闸门应与外接电源的负极相连 |
C、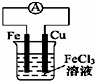 装置的总反应式是Cu+2Fe3+═Cu2++2Fe2+ |
D、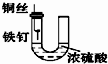 装置中的铁钉几乎没被腐蚀 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在蒸馏试验中,温度计的水银球位于蒸馏烧瓶支管口处是为了测出馏分的沸点 |
| B、在重结晶苯甲酸的试验中,步骤是:加热溶解,趁热过滤,冷却结晶 |
| C、可以用乙醇作萃取剂,提取溴水中的溴单质 |
| D、冷凝管进水口在下,出水口在上 |
查看答案和解析>>
科目:高中化学 来源: 题型:
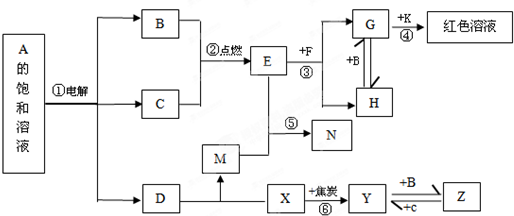
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用H2表示的反应速率为0.1mol?L-1?min-1 |
| B、用N2表示的反应速率为0.04mol?L-1?s-1 |
| C、用N2表示的反应速率为0.2mol?L-1?s-1 |
| D、用NH3表示的反应速率为0.3mol?L-1?s- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com