
| 离子 | SO42- | SO32- | NO3- | NO2- | Cl- |
| c/(mol•L-1) | 8.35×10-4 | 6.87×10-6 | 1.5×10-4 | 1.2×10-5 | 3.4×10-3 |
分析 (1)①亚氯酸钠具有氧化性,则NaClO2溶液脱硝过程中主要反应的离子方程式为3ClO2-+4NO+4OH-=4NO3-+3Cl-+2H2O;正反应是体积减小的,则增加压强,NO的转化率提高;
②根据反应的方程式3ClO2-+4NO+4OH-=4NO3-+3Cl-+2H2O可知随着吸收反应的进行氢氧根离子被消耗,吸收剂溶液的pH逐渐降低;
③由实验结果可知,在相同时间内硫酸根离子的浓度增加的多,因此脱硫反应速率大于脱硝反应速率.原因是除了SO2和NO在烟气中的初始浓度不同,还可能是二氧化硫的还原性强,易被氧化;
(2)根据反应的方程式ClO2-+2SO32-═2SO42-+Cl-可知平衡常数K表达式为K=$\frac{c(C{l}^{-})•{c}^{2}(S{O}_{4}^{2-})}{c(Cl{O}_{2}^{-})•{c}^{2}(S{O}_{3}^{2-})}$;
(3)根据盖斯定律计算.
解答 解:(1)①亚氯酸钠具有氧化性,且NaClO2溶液呈碱性,则NaClO2溶液脱硝过程中主要反应的离子方程式为3ClO2-+4NO+4OH-=4NO3-+3Cl-+2H2O;正反应是体积减小的,则增加压强,NO的转化率提高,
故答案为:3ClO2-+4NO+4OH-=4NO3-+3Cl-+2H2O;提高;
②根据反应的方程式3ClO2-+4NO+4OH-=4NO3-+3Cl-+2H2O可知随着吸收反应的进行氢氧根离子被消耗,吸收剂溶液的pH逐渐降低,
故答案为:减小;
③由实验结果可知,在相同时间内硫酸根离子的浓度增加的多,因此脱硫反应速率大于脱硝反应速率.原因是除了SO2和NO在烟气中的初始浓度不同,还可能是NO溶解度较低或脱硝反应活化能较高,
故答案为:大于;NO溶解度较低或脱硝反应活化能较高;
(2)根据反应的方程式ClO2-+2SO32-═2SO42-+Cl-可知平衡常数K表达式为K=$\frac{c(C{l}^{-})•{c}^{2}(S{O}_{4}^{2-})}{c(Cl{O}_{2}^{-})•{c}^{2}(S{O}_{3}^{2-})}$,
故答案为:$\frac{c(C{l}^{-})•{c}^{2}(S{O}_{4}^{2-})}{c(Cl{O}_{2}^{-})•{c}^{2}(S{O}_{3}^{2-})}$;
(3)已知SO2(g)+2OH-(aq)═SO32-(aq)+H2O(l)△H1
ClO-(aq)+SO32-(aq)═SO42-(aq)+Cl-(aq)△H2
CaSO4(s)═Ca2+(aq)+SO42-(aq)△H3
则根据盖斯定律可知①+②-③即得到反应SO2(g)+Ca2+(aq)+ClO-(aq)+2OH-(aq)═CaSO4(s)+H2O(l)+Cl-(aq)△H=△H1+△H2-△H3,
故答案为:△H1+△H2-△H3.
点评 本题考查氧化还原反应、盖斯定律、外界条件对反应速率和平衡状态的影响等,要求学生掌握基本概念,结合生活实际分析问题、解决问题,方程式的书写要遵循相关守恒,题目难度中等.


科目:高中化学 来源:2016-2017学年河北省高一上10月月考化学试卷(解析版) 题型:选择题
下列物质中,与0.3moLH2O含相同氢原子数的物质是
A.0.3moLHNO3 B.3.612×1023个HNO3分子
C.0.1moLH3PO4 D.0.2moLCH4
查看答案和解析>>
科目:高中化学 来源:2016-2017学年甘肃省高二上10月月考化学试卷(解析版) 题型:选择题
物质的量浓度相同的下列溶液中,NH4+浓度最大的是 ( )
A.NH4Cl B. NH4HSO4 C.CH3COONH4 D.NH4HCO3
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | a=b=c | B. | b>a>c | C. | b>c>a | D. | b=c>a |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年甘肃省高二上10月月考化学试卷(解析版) 题型:选择题
用pH试纸测定某无色溶液的pH时,规范的操作是(  )
)
A.将pH试纸放入溶液中观察其颜色变化,跟标准比色卡比较
B.将溶液倒在pH试纸上,跟标准比色卡比较
C.用干燥的洁净玻璃棒蘸取溶液,滴在pH试纸上,跟标准比色卡比较
D.在试管内放入少量溶液,煮沸,把pH试纸放在管口,观察颜色,跟标准比色卡比较
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 5Cl2+I2+6H2O═10HCl+2HIO3 | |
| B. | 2Cl2+2Ca(OH)2═CaCl2+Ca(ClO)+2H2O | |
| C. | MnO2+4HCI$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+2H2O+Cl2↑ | |
| D. | 2NaCl+2H2O $\frac{\underline{\;电解\;}}{\;}$2NaOH++Cl2↑+H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
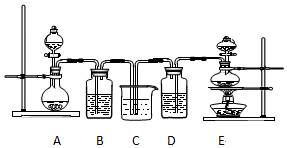

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SiO2是由极性键构成的非极性分子 | |
| B. | 若NA表示阿伏伽德罗常数,常温常压下60g SiO2中含有的共价键数目为2NA | |
| C. | 碳和硅同主族,因此CO2和SiO2化学性质相似,物理性质也相似 | |
| D. | SiO2晶体结构中的最小环为6个Si和6个O组成的12元环 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com