
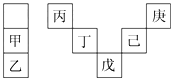
【题目】甲~庚等元素在周期表中的相对位置如表所示。己的最高价氧化物对应水化物有强脱水性,甲和丁在同一周期,甲原子最外层与最内层具有相同电子数。下列判断正确的是( )
A. 丁的最高价氧化物是人类将太阳能转换为电能的常用材料
B. 气态氢化物的稳定性:庚<己<戊
C. 常温下,甲和乙的单质均能与水剧烈反应
D. 丙与戊的原子序数相差28
【答案】D
【解析】试题分析:己的最高价氧化物对应水化物有强脱水性,则为浓硫酸,可知己为S元素,结合位置关系可知丁为Si,丙为B,庚为F,戊为As;甲和丁在同一周期,甲原子最外层与最内层具有相同电子数,则甲为Mg,可知乙为Ca元素。A.丁的最高价氧化物SiO2可用于制造光导纤维,而Si处于用作半导体材料、太阳能电池,故A错误;B.同周期自左而右非金属性增强,同主族自上而下非金属性减弱,非金属性越强,气态氢化物越稳定,则气态氢化物的稳定性:庚>己>戊,故B错误;C.金属性Ca>Mg,常温下,乙的单质能与水剧烈反应,而甲不能,故C错误;D.丙与戊的原子序数相差为33-5=28,故D正确;故选D。


科目:高中化学 来源: 题型:
【题目】下图表示各物质之间的转化关系。已知:A、B、I都是XY2型化合物,且阳离子相同,A、B晶体中阴、阳离子个数比都是1∶1,但I晶体中阴、阳离子个数比是2∶1,I常用作干燥剂。
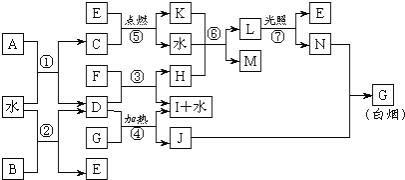
请按要求填空:
(1)I的电子式是_ __;
(2)反应⑥的化学方程式是 ,反应③在工业上的一个重要用途是 _;
(3)反应④的化学方程式是__ _;
(4)根据上图中物质之间的转化关系及题中所给信息判断,B的化学式是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯乙酸铜是合成优良催化剂、传感材料﹣纳米氧化铜的重要前驱体之一.下面是它的一种实验室合成路线:
![]() +H2O+H2SO4
+H2O+H2SO4![]()
![]() +NH4HSO4
+NH4HSO4
(苯乙腈)
![]() +Cu(OH)2→(
+Cu(OH)2→(![]() )2Cu+H2O
)2Cu+H2O
制备苯乙酸的装置示意图如图(加热和夹持装置等略):
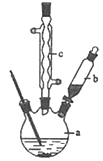
已知:苯乙酸的熔点为76.5℃,微溶于冷水,溶于乙醇.
回答下列问题:
(1)在250mL三口瓶a中加入70mL 70%硫酸.配制此硫酸时,加入蒸馏水与浓硫酸的先后顺序是 .
(2)将a中的溶液加热至100℃,缓缓滴加40g苯乙腈到硫酸溶液中,然后升温至130℃继续反应.在装置中,仪器b的作用是 ;仪器c的名称是 ,其作用是 .反应结束后加适量冷水,再分离出苯乙酸粗品.加入冷水的目的是 ,下列仪器中可用于分离苯乙酸粗品的是 (填标号)
A、分液漏斗
B、漏斗
C、烧杯
D、直形冷凝管
E、玻璃棒
(3)提纯苯乙酸的方法是重结晶,最终得到44g纯品,则苯乙酸的产率是 .(百分数)
(4)将苯乙酸加入到乙醇与水的混合溶剂中,充分溶解后,加入Cu(OH)2搅拌30min,过滤,滤液静置一段时间,析出苯乙酸铜晶体,混合溶剂中乙醇的作用是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学平衡常数K的数值大小是衡量化学反应进行程度的标志,在常温下,下列反应的平衡常数数值如下:2NO(g) ![]() N2(g)+O2(g) K1=1×1030 2H2(g)+O2(g)
N2(g)+O2(g) K1=1×1030 2H2(g)+O2(g) ![]() 2H2O(g) K2=2×1081
2H2O(g) K2=2×1081
2CO2(g) ![]() 2CO(g)+O2(g) K3=4×10-92 以下说法正确的是
2CO(g)+O2(g) K3=4×10-92 以下说法正确的是
A.常温下,NO分解产生O2的反应的平衡常数表达式为K1=c(N2)·c(O2)/ c(NO)
B.常温下,NO、H2O、CO2三种化合物分解放出O2的进行程度由大到小的顺序为NO>H2O>CO2
C.常温下,水分解产生O2,此时平衡常数的数值约为5×10-80
D.以上说法都不正确
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,用相同浓度的NaOH溶液,分别滴定100mL浓度均为0.1mol·L-1的三种酸(HM、HN和HR)溶液,滴定的曲线如图所示,下列判断错误的是
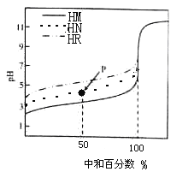
A.三种酸的电离常数关系:KHM>KHN>KHR
B.pH=7时,三种溶液中:c(M-)>c(N-)>c(R-)
C.滴定至P点时,溶液中:c(Na+)> c(N-)>c(HN)>c(H+)>c(OH-)
D.当中和百分数达100%时,将三种溶液混合后:c(HM)+c(HN)+c(HR)=c(OH-)-c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某工厂生产硼砂过程中产生的固体废料,主要含有MgCO3、MgSiO3、 CaMg(CO3)2、Al2O3和Fe2O3等,回收其中镁的工艺流程如下:

部分阳离子以氢氧化物形式完全沉淀时溶液的pH如下表,请回答下列问题:
沉淀物 | Fe3+ | Al3+ | Mg2+ |
PH | 3.2 | 5.2 | 12.4 |
(1)“浸出”步骤中,为提高镁的浸出率,可采取的措施有 (要求写出两条)。
(2)滤渣I的主要成分有 。
(3)从滤液Ⅱ中可回收利用的主要物质有 。
(4)若将MgCl2溶液加热蒸干得到的固体是__________,若要得到MgCl2应采取的操作是___________。
(5)用稀硫酸酸浸时形成滤渣的离子方程式有_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面是改良西门子法生产多晶硅的工艺流程。

(1)用惰性电极电解饱和食盐水,写出常温下X与Z反应的化学方程式 。
(2)在合成SiHCl3的过程中,还会有生成副产物SiCl4。已知两物质的沸点分别为57.6℃和31.8℃,则提纯SiHCl3的方法是 。
(3)SiHCl3提纯后用H2还原:SiHCl3(g)+H2(g) ![]() Si(s)+3HCl(g)。不同温度及不同
Si(s)+3HCl(g)。不同温度及不同![]() 时,反应物X的平衡转化率关系如图图20-1所示。
时,反应物X的平衡转化率关系如图图20-1所示。
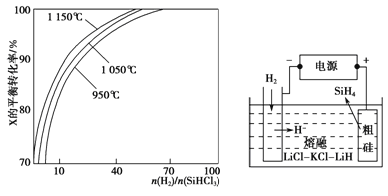
X是 (填“H2”或“SiHCl3”)。
②上述反应的平衡常数K(1150℃) K(950℃)(填“>”、“<”或“=”)。
(4)SiH4(硅烷)法生产高纯多晶硅是非常优异的方法。用粗硅作原料,熔融盐电解法制取硅烷原理如图20-2所示,电解时阳极的电极反应式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com