
【题目】在下列物质转化中,A是一种正盐,D的相对分子质量比C的相对分子质量大16,E是酸,当X无论是强酸还是强碱时,都有如下的转化关系: A ![]() B
B ![]() C
C ![]() D
D ![]() E
E
当X是强酸时,A、B、C、D、E均含同一种元素;当X是强碱时,A、B、C、D、E均含另外同一种元素.请回答:
(1)A是 .
(2)当X是强酸时,E是 . 写出B生成C的化学方程式: .
(3)当X是强碱时,E是 , 写出B生成C的化学方程式: .
【答案】
(1)(NH4)2S
(2)H2SO4;2H2S+3O2═2SO2+2H2O
(3)HNO3;4NH3+5O2 ![]() 4NO+6H2O
4NO+6H2O
【解析】解:本题中C、D的变化和D的相对分子质量比C的大16是题中一个最具有特征的条件,通过分析可初步判断D比C多一个氧原子,A为(NH4)2S,联想已构建的中学化学知识网络,符合这种转化关系的有:SO2→SO3 , NO→NO2 , Na2SO3→Na2SO4等,由此可出推断Y为O2 , 由于E为酸,则D应为能转化为酸的某物质,很可能为SO3、NO2等, 当X是强酸时A、B、C、D、E均含同一种元素,则B为H2S,C为SO2 , D为SO3 , E为H2SO4 , Z为H2O,当X是强碱时,则B为NH3 , C为NO,D为NO2 , E为HNO3 , Z为H2O,(1)本题中C、D的变化和D的相对分子质量比C的大16是题中一个最具有特征的条件,通过分析可初步判断D比C多一个氧原子可知A为(NH4)2S,
故答案为:(NH4)2S;(2)当X是强酸时,根据上面的分析可知,E是 H2SO4 , B生成C的化学方程式为2H2S+3O2═2SO2+2H2O,
故答案为:H2SO4;2H2S+3O2═2SO2+2H2O;(3)当X是强碱时,根据上面的分析可知,E是 HNO3 , B生成C的化学方程式为4NH3+5O2 ![]() 4NO+6H2O,
4NO+6H2O,
故答案为:HNO3;4NH3+5O2 ![]() 4NO+6H2O;
4NO+6H2O;
本题中C、D的变化和D的相对分子质量比C的大16是题中一个最具有特征的条件,通过分析可初步判断D比C多一个氧原子,A为(NH4)2S,联想已构建的中学化学知识网络,符合这种转化关系的有:SO2→SO3 , NO→NO2 , Na2SO3→Na2SO4等,由此可出推断Y为O2 , 由于E为酸,则D应为能转化为酸的某物质,很可能为SO3、NO2等,
当X是强酸时A、B、C、D、E均含同一种元素,则B为H2S,C为SO2 , D为SO3 , E为H2SO4 , Z为H2O,当X是强碱时,则B为NH3 , C为NO,D为NO2 , E为HNO3 , Z为H2O,据此答题;


 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值.下列判断正确的是( )
A.4.48LH2和O2的混合气体中所含分子数为0.2NA
B.标准状况下,1.8g的H2O中含有的电子数为0.1NA
C.53.5 g氯化铵晶体中含有NH ![]() 的数目为NA
的数目为NA
D.标准状况下,22.4 L氦气所含有的原子数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】含有重金属离子的废水直接排入水体,会导致水生动物中毒,毒性的表现与离子浓度和染毒时间正相关。为了验证铅离子对鲫鱼肝胰脏细胞内过氧化氢酶活性的影响,请根据以下提供的材料和用具,完善实验思路,预测实验结果并进行分析。
材料与用具:鲫鱼、铅染毒溶液、匀浆器、试管、H2O2磷酸缓冲液等。
(要求和说明:H2O2磷酸缓冲液由H2O2和磷酸缓冲液组成,其中的H2O2含量可用光电比色法测定,具体检测过程不要求写出)
请回答:
(1)实验思路:
①染毒饲养:取3个水族箱,分别加入等量铅浓度为0、20、40mg/L的铅染毒溶液,每个水族箱饲养20尾鲫鱼。
②制备酶液:染毒开始时及过程中每隔24小时,每组捕捉4尾鲫鱼,取每尾鱼的肝胰脏 0.5g打成匀浆,并制备成酶提取液。
③测酶活性:取试管加入 和 ,反应3分钟立即测定试管中的 。
④ 。
(2)预测实验结果:(在坐标系中用柱状图表示第1次、第5次的实验结果)

(3)分析与讨论:
① 下列关于将肝胰脏制备成酶提取液的叙述错误的是 。
A.将肝胰脏打成匀浆有利于提取酶
B.应该将0.5g克肝胰脏制备成等体积的酶液
C.提取的酶液应该加入磷酸缓冲液并低温保存
D.直接使用匀浆进行实验对实验结果没有影响
② 将H2O2配制成H2O2磷酸缓冲液是为了保证反应过程中的 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有四种短周期元素,它们的结构、性质等信息如下表所述:
元素 | 结构、性质等信息 |
A | 是短周期中(除稀有气体外)原子半径最大的元素,该元素的某种合金是原子反应堆的导热剂 |
B | B与A同周期,其最高价氧化物的水化物呈两性 |
C | 元素的气态氢化物极易溶于水,可用作制冷剂 |
D | 是海水中除氢、氧元素外含量最多的元素,其单质或化合物也是自来水生产过程中常用的消毒杀菌剂 |
请根据表中信息填写:
(1)A原子的核外电子排布式为 .
(2)B元素在周期表中的位置为;离子半径:BA(填“大于”或“小于”).
(3)C原子的电子排布图是 , 其原子核外有个未成对电子,能量最高的电子为轨道上的电子,其轨道呈形.
(4)D原子的电子排布式为 , D﹣的结构示意图是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)为了防止氯化亚铁溶液氧化变质,常在其中加入____,反应的离子方程式是_____;
(2)除去铁粉中的铝粉,可用过量的_______溶液,然后过滤,反应化学方程式为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由1分子的磷酸、碱基m和化合物a构成了化合物b,如下图所示。下列相关叙述中正确的是
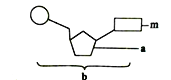
A. 若m为胸腺嘧啶,则b肯定为脱氧核糖
B. 若b为组成核糖体的成分,则b只有4种
C. 若ATP水解可形成b,则a为核糖核苷酸
D. 若a为核糖,则a和磷酸交替排列构成了DNA的基本骨架
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是部分短周期元素化合价与原子序数的关系图,下列说法正确的是( ) 
A.原子半径:Z>Y>X
B.气态氢化物的稳定性:R>W
C.WX3和水反应形成的化合物是离子化合物
D.Y和Z两者最高价氧化物对应的水化物的碱性:Y<Z
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图示为某20肽,其中含天门冬氨酸4个,分别位于第5、6、15、20位;肽酶X专门作用于天门冬氨酸羧基端的肽键,肽酶Y专门作用于天门冬氨酸氨基端的肽键,下列相关叙述正确的是( )

A. 该20肽含有肽键数为20个
B. 该20肽游离的氨基和羧基各为1个和5个
C. 肽酶X完全作用后产生的多肽共含有氨基酸18个
D. 肽酶Y完全作用后产生的多肽中氧原子数目比20肽少4个
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com